Термодинамічні принципи
Щоб легше зрозуміти широкий і складний світ термодинаміки, рекомендується йти поетапно, починаючи з огляду основних термінів, вступу до термодинамічних принципів, а потім глибше вивчаючи термодинамічні закони, як вони виражаються математично. та його застосування.
У чотирьох законах термодинаміки (нульовий закон, перший закон, другий закон і третій закон) описано, як працюють передачі та перетворення енергії між різними системами; будучи основою для розуміння багатьох фізико-хімічних явищ природи.
Огляд основних понять
Запрошуємо переглянути статтю ТЕРМОДИНАМІКА, що це таке та її застосування

Ви можете доповнити цю інформацію статтею Сила закону Ватта (додатки - вправи) Поки МИ СЛЕДУЄМО ...
Форми енергії
Енергія, властивість тіл перетворювати себе, змінюючи своє становище або стан, має різні форми, наприклад кінетична енергія, потенційна енергія та внутрішня енергія тіл. Дивіться малюнок 1.
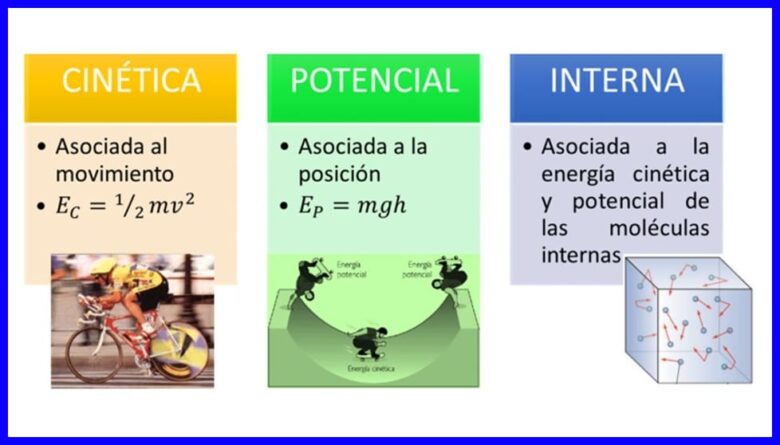
Працювати
Це добуток сили та переміщення, які вимірюються в одному напрямку. Для розрахунку роботи використовується складова сили, паралельна зміщенню об’єкта. Робота вимірюється в Нм, Джоулях (J), футах-фунтів-ф або BTU. Дивіться малюнок 2.
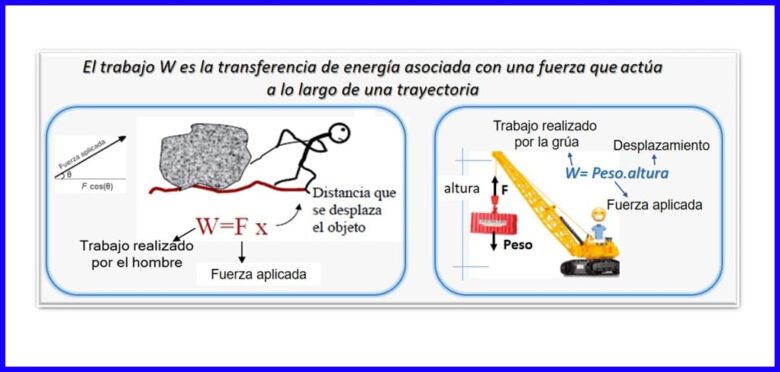
Тепло (Q)
Передача теплової енергії між двома тілами, які перебувають при різних температурах, і відбувається це лише в тому сенсі, що температура знижується. Тепло вимірюється в Джоулях, BTU, фунт-футах або в калоріях. Дивіться малюнок 3.
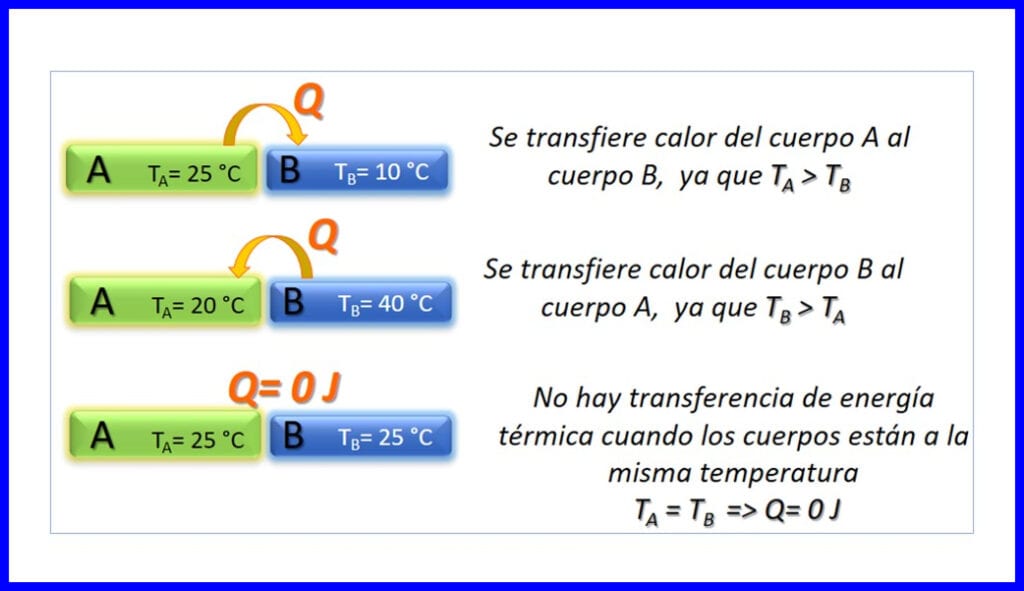
Термодинамічні принципи
Нульовий Закон - Нульовий Принцип
Нульовий закон термодинаміки стверджує, що якщо два об'єкти, A і B, перебувають в тепловій рівновазі один з одним, а об'єкт A знаходиться в рівновазі з третім об'єктом C, то об'єкт B знаходиться в тепловій рівновазі з об'єктом C. Настає теплова рівновага коли два або більше тіл мають однакову температуру. Дивіться малюнок 4.
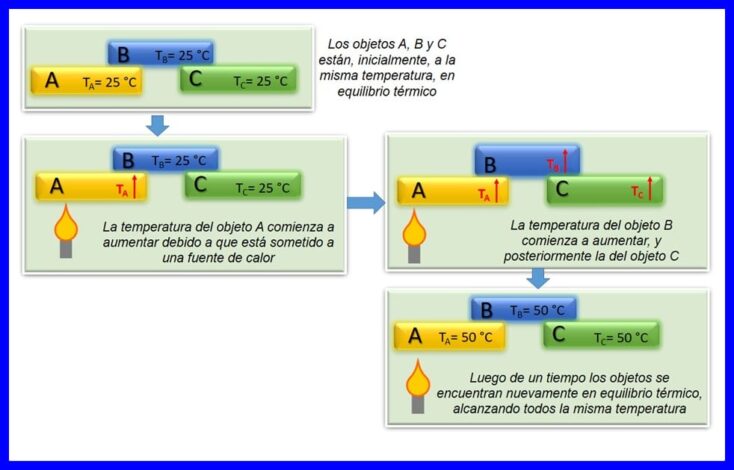
Цей закон вважається основним законом термодинаміки. Він був постульований як "Нульовий Закон" в 1935 році, оскільки він був постульований після створення першого та другого законів термодинаміки.
1-й закон термодинаміки (Принцип збереження енергії)
Постанова Першого закону термодинаміки:
Перший закон термодинаміки, також відомий як принцип збереження енергії, стверджує, що енергія не створюється і не руйнується, вона лише трансформується в інший тип енергії, або вона передається від одного об’єкта до іншого. Таким чином, загальна кількість енергії у Всесвіті не змінюється.
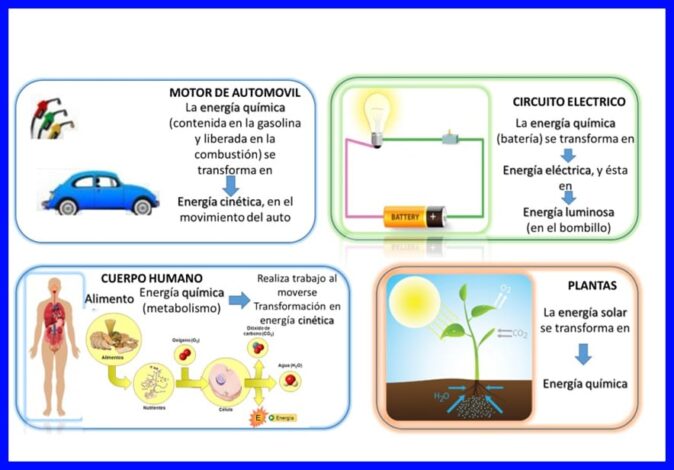
Перший закон виконується у всьому, енергія передається і перетворюється безперервно, наприклад, в деяких електричних приладах, таких як змішувачі та блендери, електрична енергія перетворюється на механічну та теплову енергію, в організмі людини вони перетворюють хімічну енергія їжі, яка потрапляє в кінетичну енергію, коли тіло знаходиться в русі, або інші приклади, такі як наведені на малюнку 5.
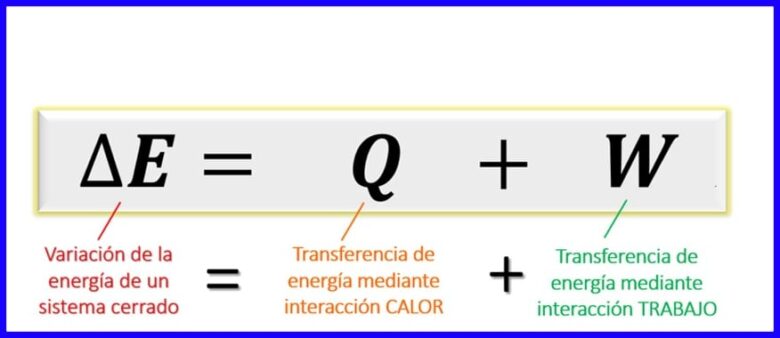
Рівняння першого закону термодинаміки:
Рівняння першого закону в рамках термодинамічних принципів виражає баланс, який повинен існувати між різними типами енергії в даному процесі. Оскільки в закритих системах [1] обмін енергією може бути заданий лише за рахунок передачі тепла або виконаної роботи (системою або системою), встановлено, що зміна енергії системи дорівнює сумі передачі енергії через тепло і через роботу. Дивіться малюнок 6.
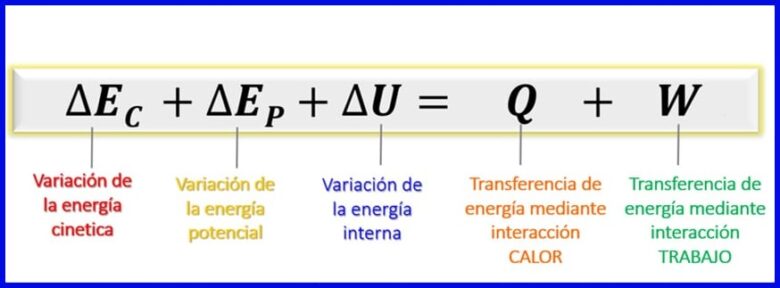
Враховуючи, що енергії, що розглядаються в цьому енергетичному балансі, є кінетичною енергією, потенційною енергією та внутрішньою енергією [1], енергетичний баланс для закритих систем залишається таким, як показано на рисунку 7.
- (Ек) Кінетична енергія , внаслідок руху тіла;
- (Еп) Потенційна енергія, завдяки положенню тіла в гравітаційному полі;
- (АБО) Внутрішня енергія, завдяки мікроскопічним внескам кінетичної та потенційної енергії внутрішніх молекул тіла.
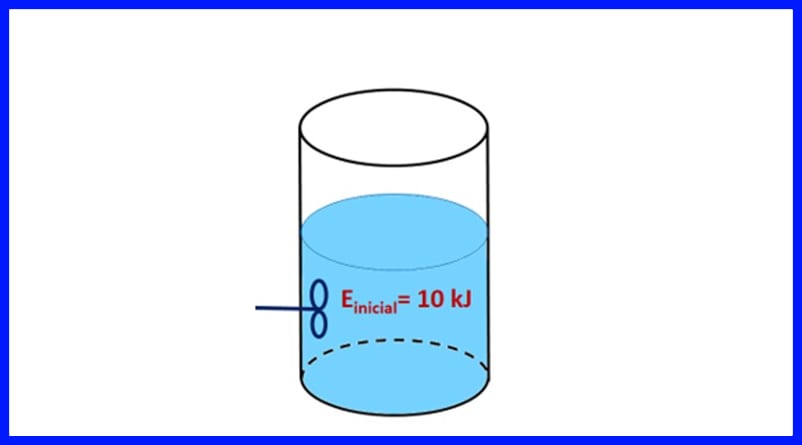
Вправа 1.
Герметичний контейнер містить речовину з початковою енергією 10 кДж. Речовину перемішують пропелером, який працює 500 Дж, тоді як джерело тепла передає речовині 20 кДж тепла. Крім того, під час процесу в повітря виділяється 3 кДж тепла. Визначте кінцеву енергію речовини. Дивіться малюнок 8.
рішення:
На малюнку 9 ви можете побачити тепло, додане джерелом тепла, яке вважається "позитивним", оскільки воно збільшує енергію речовини, тепло, що виділяється в повітря, негативним, оскільки зменшує енергію речовини, і Робота гвинта, що збільшила енергію, прийняла позитивний знак.
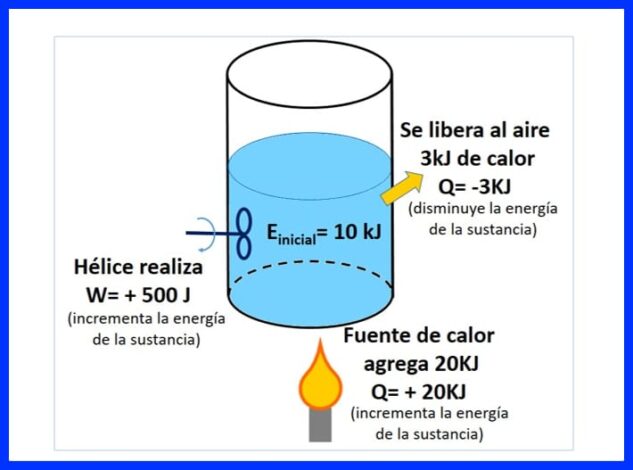
На рисунку 10 представлений енергетичний баланс згідно з першим законом термодинаміки та отримана кінцева енергія речовини.

Другий закон термодинаміки
Існує кілька тверджень другого закону термодинаміки: Заява Планка-Кельвіна, Клаузіуса, Карно. Кожен з них показує різний аспект другого закону. Загалом другий закон термодинаміки постулює:
- Напрямок термодинамічних процесів, незворотність фізичних явищ.
- Ефективність роботи теплових машин.
- Введіть властивість "ентропія".
Напрямок термодинамічних процесів:
Спонтанно в природі енергія перетікає або переходить із вищого енергетичного стану в найнижчий енергетичний стан. Тепло надходить від гарячих тіл до холодних, а не навпаки. Див. Малюнок 11.

Ефективність або теплові характеристики:
Згідно з першим законом термодинаміки, енергія не створюється і не руйнується, але вона може перетворюватися або передаватися. Але при будь-яких передачах енергії або перетвореннях їх кількість не є корисною для виконання роботи. У міру передачі або перетворення енергії частина початкової енергії виділяється як теплова енергія: енергія деградує, втрачає якість.
При будь-якому перетворенні енергії кількість отриманої енергії завжди менше енергії, що подається. Теплова ефективність - це кількість тепла від джерела, яке перетворюється на роботу, співвідношення між корисною енергією, що отримується, та енергією, що надходить при перетворенні. Див. Малюнок 12.

Теплова машина або Теплова машина:
Теплова машина - це пристрій, який частково перетворює тепло в робочу або механічну енергію, для цього йому потрібно джерело, що подає тепло при високій температурі.
У теплових машинах використовується така речовина, як водяна пара, повітря або паливо. Речовина циклічно піддається серії термодинамічних перетворень, завдяки чому машина може працювати безперервно.
Вправа 2.
Двигун вантажного автомобіля виробляє тепло при згорянні, спалюючи бензин. Для кожного циклу двигуна теплота 5 кДж перетворюється на 1 кДж механічної роботи. Який ККД двигуна? Скільки теплоти виділяється за кожен цикл двигуна? Дивіться малюнок 13
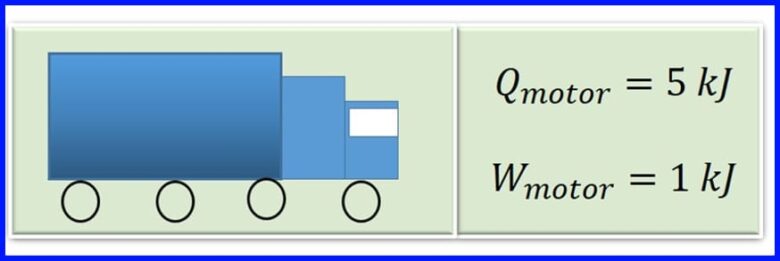
рішення:

Для визначення виділеного тепла передбачається, що в теплових машинах чиста робота дорівнює чистому теплопередачі в систему. Дивіться малюнок 14.

Ентропія:
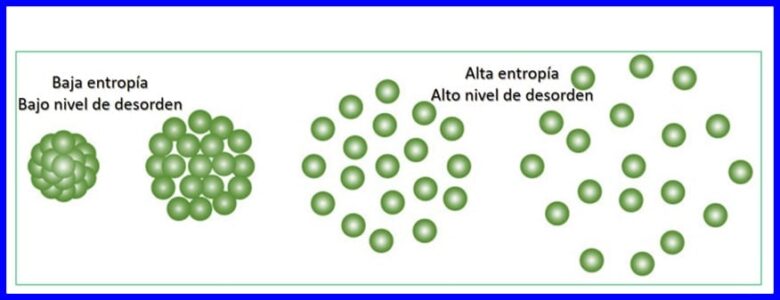
Ентропія - це ступінь випадковості або розладу в системі. Ентропія дозволяє кількісно визначити частину енергії, яка не може бути використана для виробництва роботи, тобто дозволяє кількісно визначити незворотність термодинамічного процесу.
Кожен перенос енергії, що відбувається, збільшує ентропію Всесвіту та зменшує кількість корисної енергії, доступної для роботи. Будь-який термодинамічний процес буде проходити у напрямку, що збільшує загальну ентропію Всесвіту. Див. Малюнок 15.
3-й закон термодинаміки
Третій закон термодинаміки або Нерстський постулат
Третій закон термодинаміки пов’язаний з температурою та охолодженням. Він стверджує, що ентропія системи за абсолютним нулем є певною константою. Див. Малюнок 16.
Абсолютний нуль - це найнижча температура, нижче якої не існує нижчої міри, це найхолодніше, що може бути тіло. Абсолютний нуль дорівнює 0 K, що еквівалентно -273,15 ºC.

Висновок
Існує чотири термодинамічні принципи. За нульовим принципом встановлено, що теплова рівновага настає, коли два або більше тіл мають однакову температуру.
Перший закон термодинаміки стосується збереження енергії між процесами, тоді як другий закон термодинаміки стосується спрямованості від найнижчої до найвищої ентропії, а також ефективності або продуктивності теплових двигунів, які перетворюють тепло в роботу.
Третій закон термодинаміки пов'язаний з температурою та охолодженням, він стверджує, що ентропія системи при абсолютному нулі є певною константою.