Termodinamična načela
Da bi na enostaven način razumeli širok in zapleten svet termodinamike, je priporočljivo iti korak za korakom, začenši s pregledom osnovnih izrazov, uvodom v termodinamične principe in nato poglobljeno preučevanjem termodinamičnih zakonov, kako so izraženi matematično in njegove aplikacije.
S štirimi zakoni termodinamike (ničelni zakon, prvi zakon, drugi zakon in tretji zakon) je opisano, kako delujejo prenosi in pretvorbe energije med različnimi sistemi; je osnova za razumevanje številnih fizikalno-kemijskih pojavov v naravi.
Pregled osnovnih konceptov
Vabimo vas, da si ogledate članek TERMODINAMIKA, kaj je in njene uporabe

Te podatke lahko dopolnite s člankom Moč Wattovega zakona (aplikacije - vaje) Za zdaj Sledimo ...
Oblike energije
Energija, lastnost teles, da se preoblikujejo s spreminjanjem svojega stanja ali stanja, je v številnih oblikah, kot npr kinetična energija, potencialna energija in notranja energija teles. Glej sliko 1.
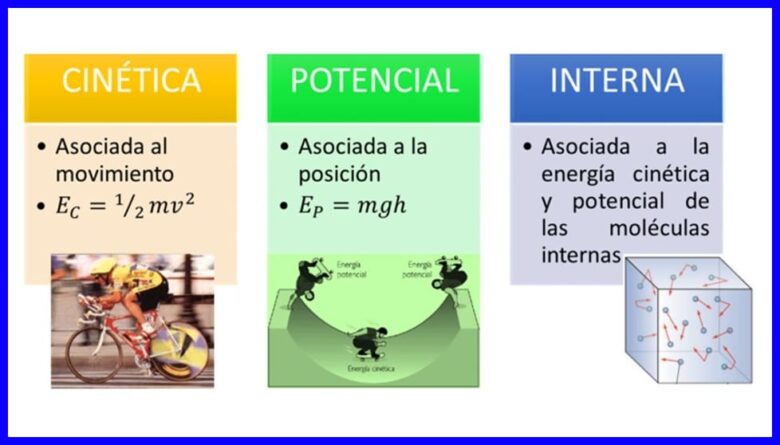
Delo
Je produkt sile in premika, ki se merita v isti smeri. Za izračun dela se uporabi komponenta sile, ki je vzporedna z odmikom predmeta. Delo se meri v Nm, Joule (J), ft.lb-f ali BTU. Glej sliko 2.
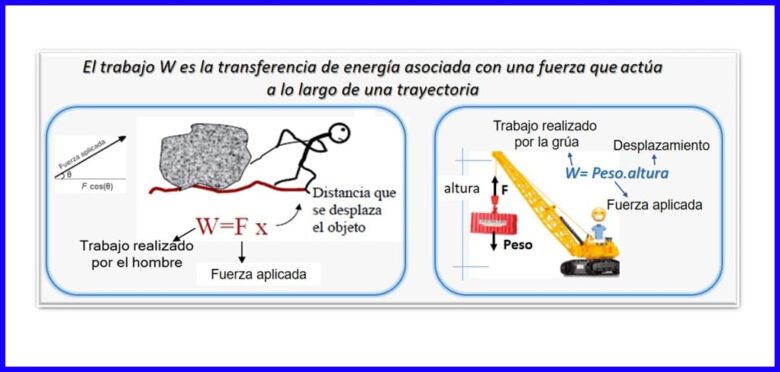
Vročina (Q)
Prenos toplotne energije med dvema telesoma, ki imata različno temperaturo, in se zgodi le v smislu, da se temperatura zmanjša. Toplota se meri v džulih, BTU, kilogramih ali kalorijah. Glej sliko 3.
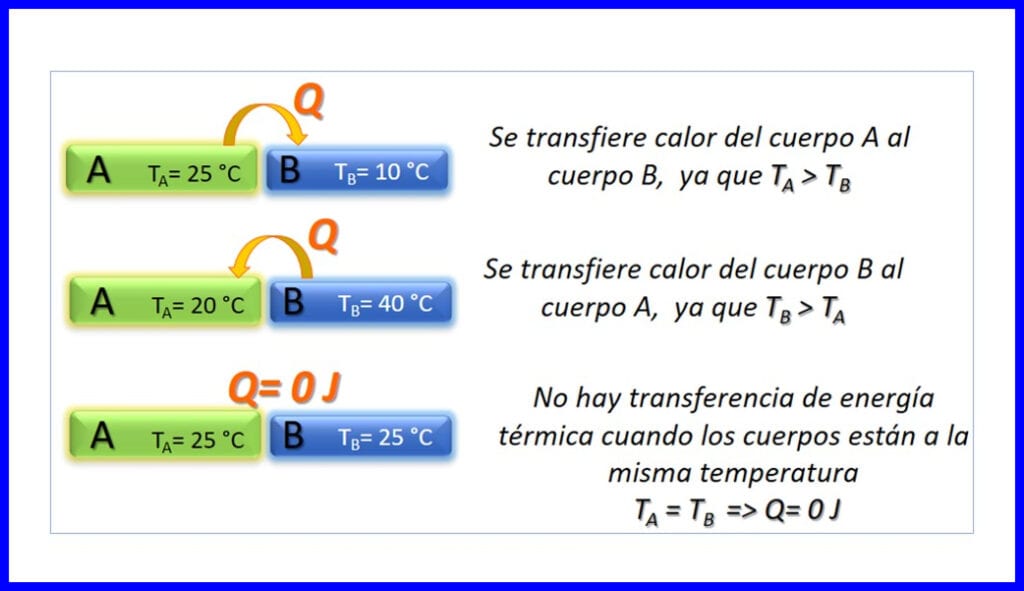
Termodinamična načela
Nič zakon - ničelno načelo
Ničelni zakon termodinamike pravi, da če sta dva predmeta, A in B, medsebojno v toplotnem ravnovesju in je objekt A v ravnovesju s tretjim objektom C, potem je objekt B v toplotnem ravnovesju s predmetom C. Termično ravnovesje nastopi ko sta dve ali več teles enake temperature. Glej sliko 4.
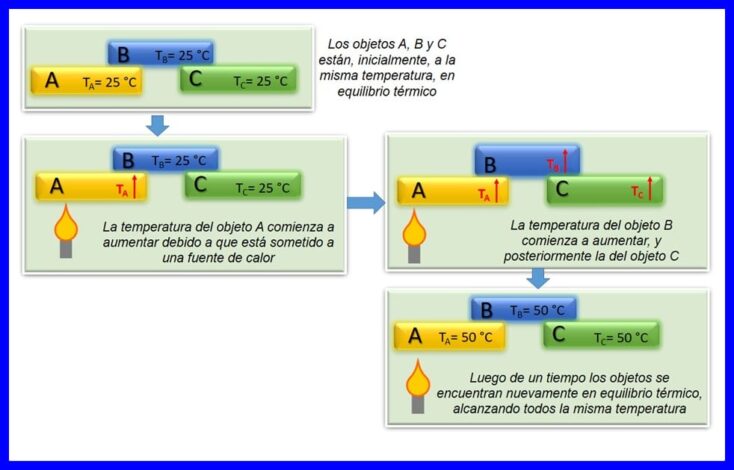
Ta zakon velja za osnovni zakon termodinamike. Leta 1935 je bil postavljen kot "ničelni zakon", saj je bil postavljen po prvem in drugem zakonu termodinamike.
1. zakon termodinamike (načelo ohranjanja energije)
Izjava o prvem termodinamičnem zakonu:
Prvi zakon termodinamike, znan tudi kot načelo ohranjanja energije, pravi, da se energija ne ustvarja ali uničuje, le pretvori se v drugo vrsto energije ali pa se prenaša z enega predmeta na drugega. Tako se celotna količina energije v vesolju ne spremeni.
Prvi zakon je izpolnjen v "vsem", energija se neprestano prenaša in preoblikuje, na primer v nekaterih električnih napravah, kot so mešalniki in mešalniki, električna energija se pretvori v mehansko in toplotno energijo, v človeškem telesu pa kemikalije energija hrane, ki se zaužije v kinetično energijo, ko je telo v gibanju, ali drugi primeri, kot so prikazani na sliki 5.
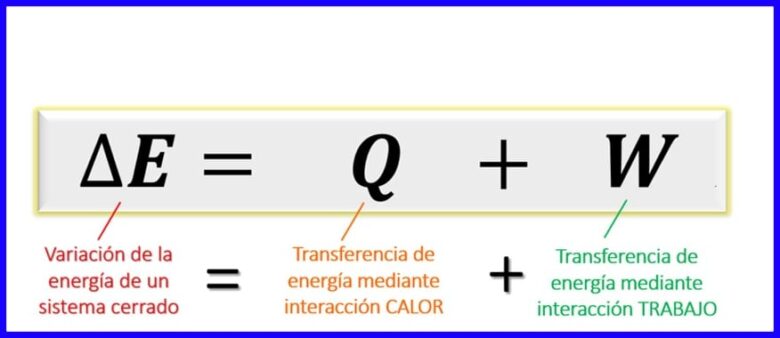
Enačba prvega zakona termodinamike:
Enačba prvega zakona znotraj termodinamičnih načel izraža ravnovesje, ki mora obstajati med različnimi vrstami energije v danem procesu. Ker je v zaprtih sistemih [1] izmenjavo energije mogoče dati samo s prenosom toplote ali z opravljenim delom (s sistemom ali na njem), je ugotovljeno, da je sprememba energije sistema enaka vsoti prenos energije skozi toploto in z delom. Glej sliko 6.
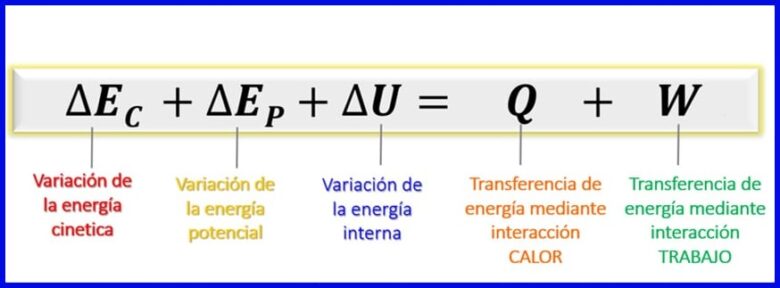
Glede na to, da so energije, upoštevane v tej energetski bilanci, kinetična, potencialna in notranja energija [1], ostaja energetska bilanca za zaprte sisteme, kot je prikazano na sliki 7.
- (ec) Kinetična energija , zaradi gibanja telesa;
- (ep) Potencialna energija, zaradi položaja telesa v gravitacijskem polju;
- (ALI) Notranja energija, zaradi mikroskopskih prispevkov kinetične in potencialne energije notranjih molekul telesa.
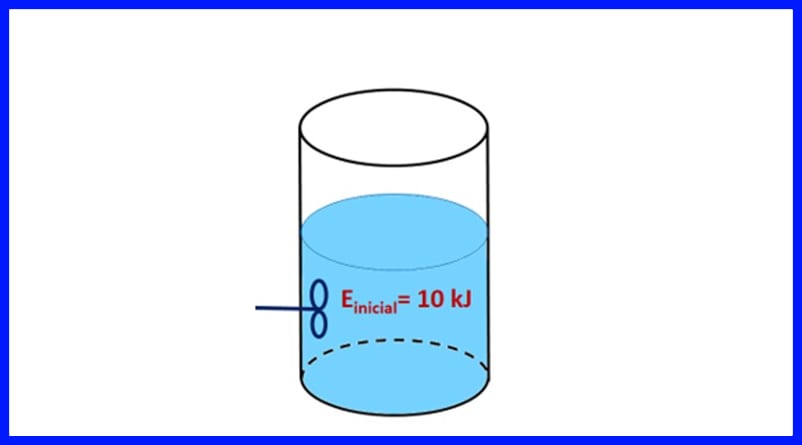
Vaja 1.
Zaprta posoda vsebuje snov z začetno energijo 10 kJ. Snov mešamo s propelerjem, ki deluje 500 J, vir toplote pa prenaša 20 kJ toplote na snov. Poleg tega se med postopkom v zrak sprosti 3kJ toplote. Določite končno energijo snovi. Glej sliko 8.
rešitev:
Na sliki 9 lahko vidite toploto, ki jo doda vir toplote, kar velja za "pozitivno", saj povečuje energijo snovi, toploto, ki se sprošča v zrak, negativno, saj zmanjšuje energijo snovi, in delo propelerja, ki je povečalo energijo, je dobilo pozitiven znak.
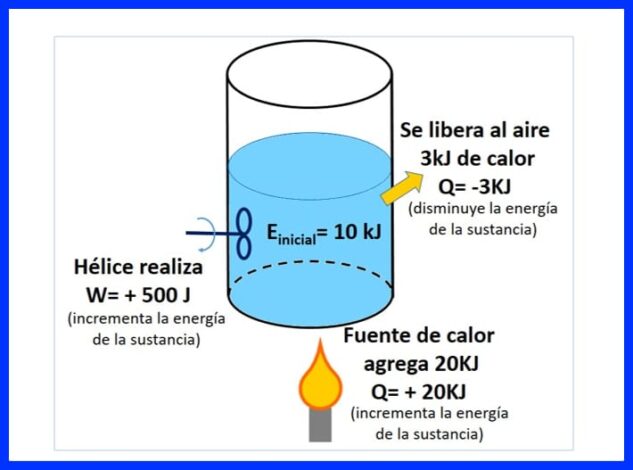
Na sliki 10 je predstavljena energijska bilanca v skladu s prvim termodinamičnim zakonom in končna energija snovi.

Drugi zakon termodinamike
Obstaja več izjav drugega zakona termodinamike: Izjava Planck-Kelvin, Clausius, Carnot. Vsak od njih kaže drugačen vidik drugega zakona. Na splošno velja drugi zakon termodinamike:
- Smer termodinamičnih procesov, nepovratnost fizikalnih pojavov.
- Učinkovitost termičnih strojev.
- Vnesite lastnost "entropija".
Smer termodinamičnih procesov:
Spontano v naravi energija teče ali se prenaša iz najvišjega v najnižje. Toplota prehaja iz vročih teles v hladna telesa in ne obratno. Glej sliko 11.

Učinkovitost ali toplotna zmogljivost:
Po prvem termodinamičnem zakonu energija ni niti ustvarjena niti uničena, ampak jo je mogoče transformirati ali prenesti. Toda pri vseh prenosih ali preoblikovanjih energije dela ni koristno opravljati. Ko se energija prenaša ali transformira, se del začetne energije sprosti kot toplotna energija: energija se razgradi in izgubi kakovost.
Pri kateri koli energetski preobrazbi je količina pridobljene energije vedno manjša od dovedene energije. Toplotna učinkovitost je količina toplote iz vira, ki se pretvori v delo, razmerje med pridobljeno koristno in dovedeno energijo pri transformaciji. Glej sliko 12.

Termični ali toplotni stroj:
Termalni stroj je naprava, ki toploto delno pretvori v delovno ali mehansko energijo, za kar potrebuje vir, ki toploto oskrbuje pri visoki temperaturi.
V termičnih strojih se uporablja snov, kot so vodna para, zrak ali gorivo. Snov ciklično prehaja v vrsto termodinamičnih pretvorb, tako da lahko stroj neprekinjeno deluje.
Vaja 2.
Motor tovornega vozila pri zgorevanju bencina proizvaja toploto pri zgorevanju. Za vsak cikel motorja se toplota 5 kJ pretvori v 1kJ mehanskega dela. Kolikšen je izkoristek motorja? Koliko toplote se sprosti za vsak cikel motorja? Glej sliko 13
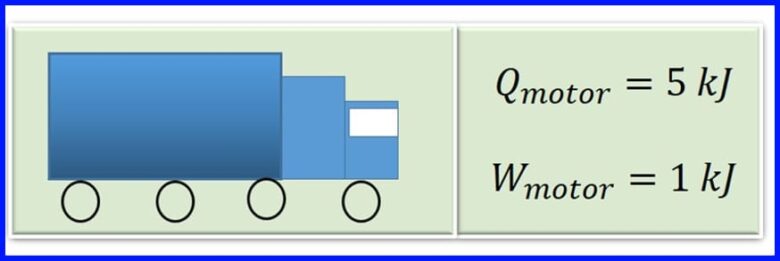
rešitev:

Za določitev sproščene toplote se predpostavlja, da je v termičnih strojih neto delo enako neto prenosu toplote v sistem. Glej sliko 14.

Entropija:
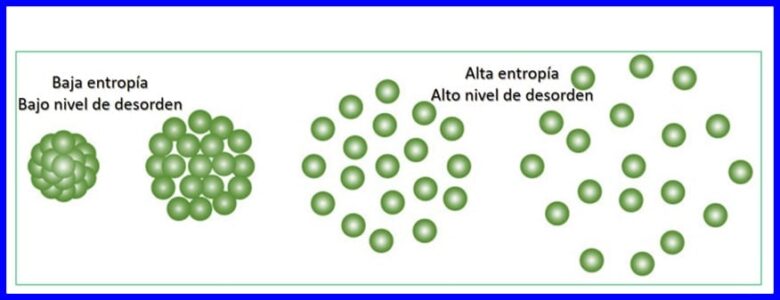
Entropija je stopnja naključnosti ali motnje v sistemu. Entropija omogoča količinsko opredelitev dela energije, ki je ni mogoče uporabiti za izdelavo dela, to pomeni, da omogoča količinsko določitev nepovratnosti termodinamičnega procesa.
Vsak prenos energije, ki se zgodi, poveča entropijo vesolja in zmanjša količino uporabne energije, ki je na voljo za delo. Vsak termodinamični proces bo potekal v smeri, ki povečuje celotno entropijo vesolja. Glej sliko 15.
3. zakon termodinamike
Tretji zakon termodinamike ali Nerstovega postulata
Tretji zakon termodinamike je povezan s temperaturo in hlajenjem. Navaja, da je entropija sistema pri absolutni ničli določena konstanta. Glej sliko 16.
Absolutna ničla je najnižja temperatura, pod katero ni več nižje mere, je najhladnejše, kar je lahko telo. Absolutna ničla je 0 K, kar ustreza -273,15 ºC.

Zaključek
Obstajajo štirje termodinamični principi. V principu nič je ugotovljeno, da pride do toplotnega ravnovesja, ko sta dve ali več teles enake temperature.
Prvi zakon termodinamike obravnava ohranjanje energije med procesi, drugi zakon termodinamike pa usmerjenost od najnižje do najvišje entropije ter učinkovitost ali delovanje toplotnih strojev, ki toploto pretvarjajo v delo.
Tretji zakon termodinamike je povezan s temperaturo in hlajenjem, pravi, da je entropija sistema pri absolutni ničli določena konstanta.