Termodynamické princípy
Aby sme jednoduchým spôsobom pochopili široký a zložitý svet termodynamiky, odporúča sa ísť krok za krokom, počnúc prehľadom základných pojmov, úvodom do termodynamických princípov, až po hlbšie štúdium termodynamických zákonov, ako sú vyjadrené matematicky a jeho aplikácie.
So štyrmi zákonmi termodynamiky (nulový zákon, prvý zákon, druhý zákon a tretí zákon) je opísané, ako fungujú prenosy a transformácie energie medzi rôznymi systémami; je základom pre pochopenie mnohých fyzikálno-chemických javov prírody.
Preskúmanie základných pojmov
Pozývame vás pozrieť si článok TERMODYNAMIKA, čo to je a jej aplikácie

Tieto informácie môžete doplniť článkom Sila Wattovho zákona (Aplikácie - Cvičenia) V súčasnej dobe SLEDUJEME ...
Formy energie
Energia, vlastnosť telies, ktoré sa môžu transformovať úpravou svojej situácie alebo stavu, má mnoho podôb, ako napr kinetická energia, potenciálna energia a vnútorná energia telies. Pozri obrázok 1.
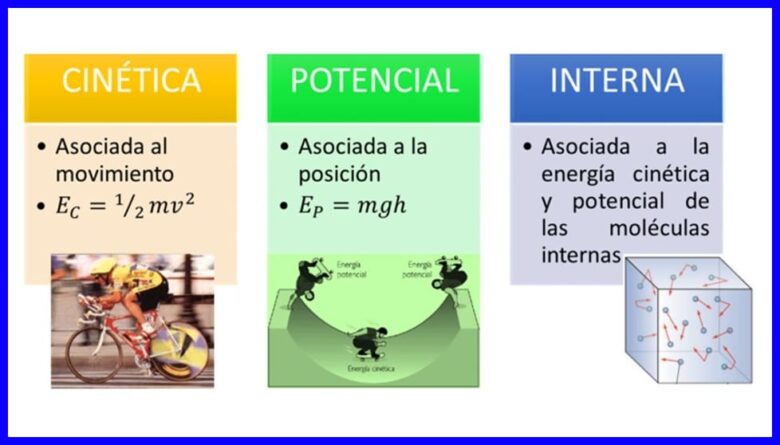
Práce
Je to produkt sily a posunu, ktoré sa merajú v rovnakom smere. Na výpočet práce sa používa zložka sily, ktorá je rovnobežná s posunom objektu. Práca sa meria v Nm, Joule (J), ft.lb-f alebo BTU. Pozri obrázok 2.
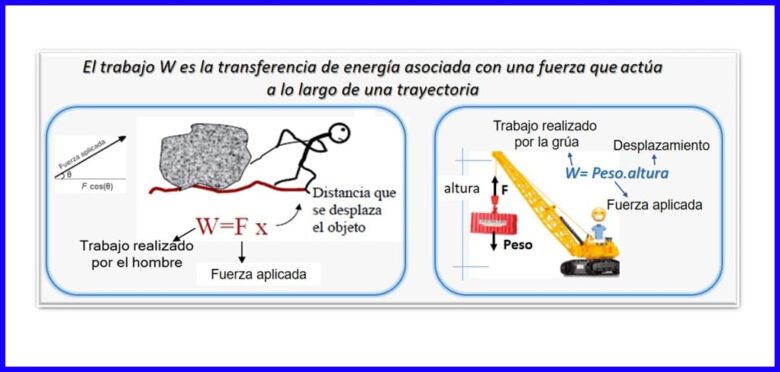
Teplo (Q)
Prenos tepelnej energie medzi dvoma telesami, ktoré majú rôzne teploty, a to iba v tom zmysle, že teplota klesá. Teplo sa meria v Joule, BTU, libre stôp alebo v kalóriách. Pozri obrázok 3.
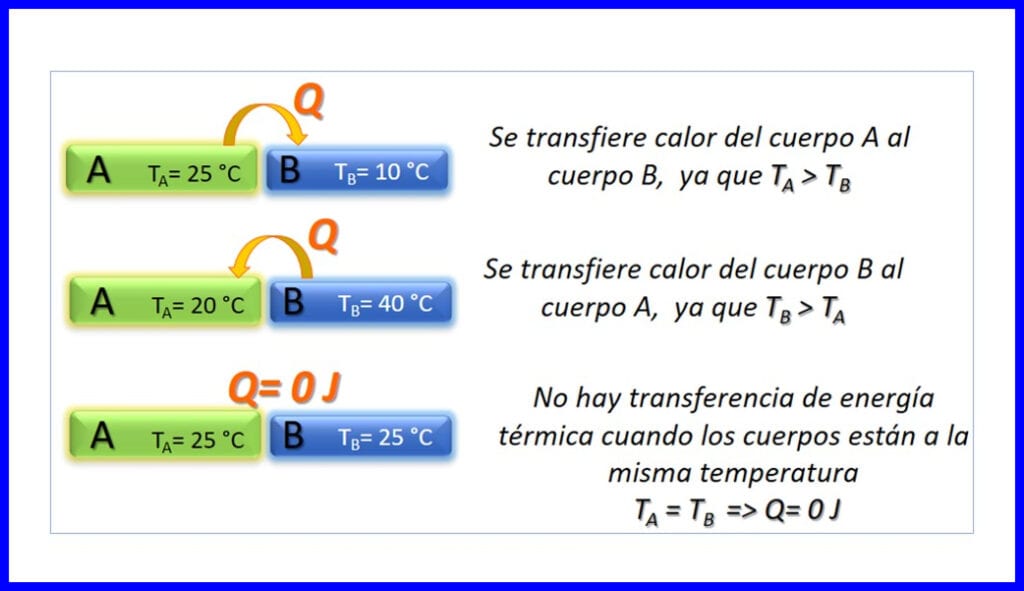
Termodynamické princípy
Nulový zákon - nulový princíp
Nulový zákon termodynamiky hovorí, že ak sú dva objekty A a B navzájom v tepelnej rovnováhe a objekt A je v rovnováhe s tretím objektom C, potom je objekt B v tepelnej rovnováhe s objektom C. Dochádza k tepelnej rovnováhe keď majú dve alebo viac telies rovnakú teplotu. Pozri obrázok 4.
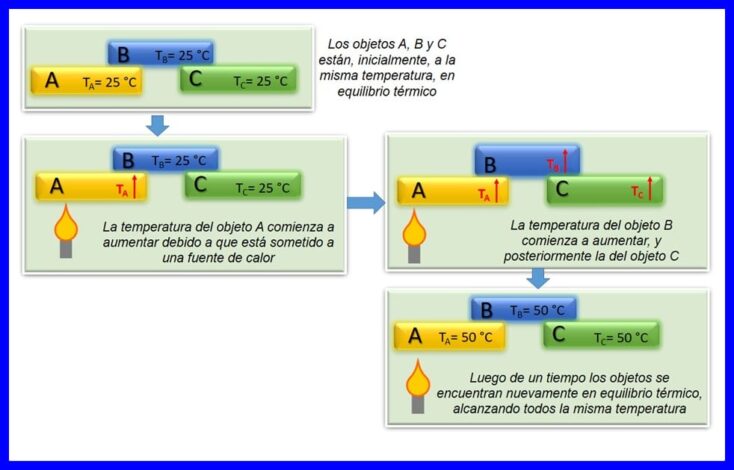
Tento zákon sa považuje za základný zákon termodynamiky. To bolo postulované ako „nulový zákon“ v roku 1935, pretože to bolo postulované po vytvorení prvého a druhého zákona termodynamiky.
1. zákon termodynamiky (princíp úspory energie)
Vyhlásenie prvého termodynamického zákona:
Prvý zákon termodynamiky, tiež známy ako princíp zachovania energie, hovorí, že energia sa netvorí ani nezničí, iba sa transformuje na iný druh energie alebo sa prenáša z jedného objektu do druhého. Celkové množstvo energie vo vesmíre sa teda nemení.
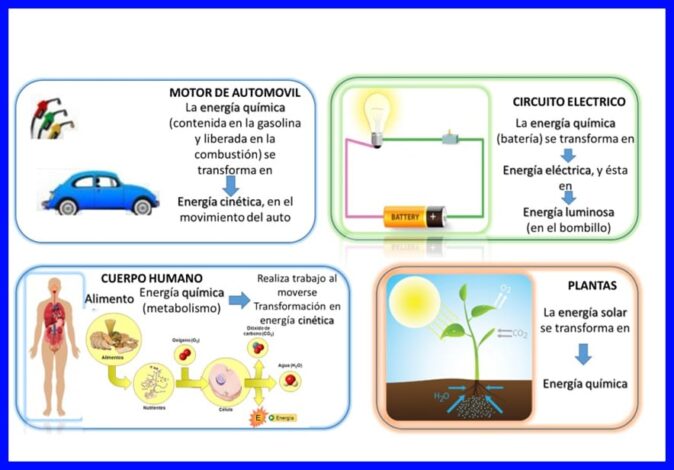
Prvý zákon je splnený vo „všetkom“, energia sa prenáša a transformuje nepretržite, napríklad v niektorých elektrických zariadeniach, ako sú mixéry a mixéry, sa elektrická energia transformuje na mechanickú a tepelnú energiu, v ľudskom tele sa transformujú chemická látka energia jedla, ktorá sa prijme do kinetickej energie, keď je telo v pohybe, alebo ďalšie príklady, ako sú napríklad tie, ktoré sú znázornené na obrázku 5.
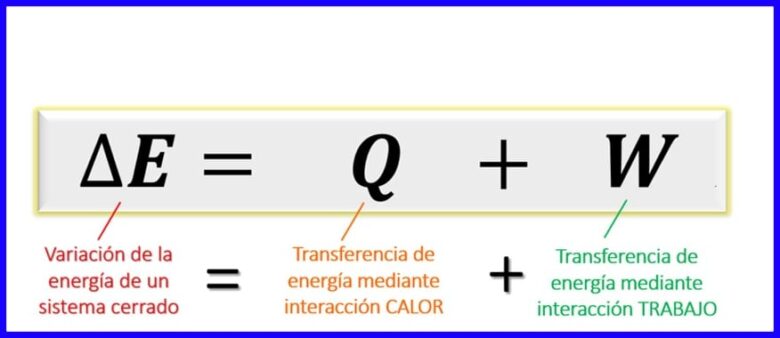
Rovnica prvého termodynamického zákona:
Rovnica prvého zákona v termodynamických princípoch vyjadruje rovnováhu, ktorá musí existovať medzi rôznymi druhmi energie v danom procese. Pretože v uzavretých systémoch [1] môžu byť výmeny energie dané iba prestupom tepla alebo vykonanou prácou (systémom alebo na systéme), je dokázané, že energetická zmena systému sa rovná súčtu prenosu energie teplom a prácou. Pozri obrázok 6.
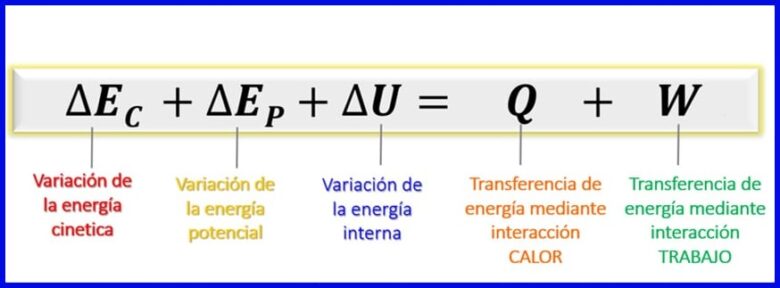
Ak vezmeme do úvahy, že energie uvažované v tejto energetickej bilancii sú kinetická energia, potenciálna energia a vnútorná energia [1], zostáva energetická bilancia pre uzavreté systémy taká, ako je to znázornené na obrázku 7.
- (ec) Kinetická energia , v dôsledku pohybu tela;
- (ep) Potenciálna energia, v dôsledku polohy telesa v gravitačnom poli;
- (OR) Vnútorná energia, v dôsledku mikroskopických príspevkov kinetickej a potenciálnej energie vnútorných molekúl tela.
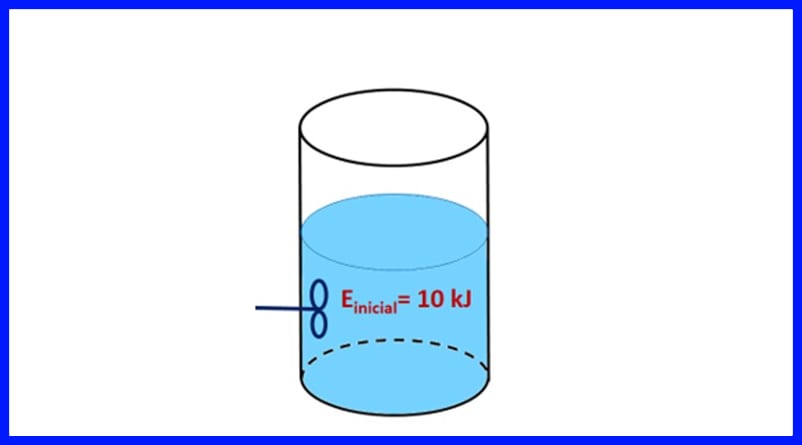
Cvičenie 1.
Zapečatená nádoba obsahuje látku s počiatočnou energiou 10 kJ. Látka sa mieša s vrtuľou, ktorá pracuje 500 J, zatiaľ čo zdroj tepla prenáša na látku 20 kJ tepla. Počas procesu sa navyše do ovzdušia uvoľňujú 3 kJ tepla. Určte konečnú energiu látky. Pozri obrázok 8.
riešenie:
Na obrázku 9 vidíte teplo pridané zdrojom tepla, ktoré sa považuje za „pozitívne“, pretože zvyšuje energiu látky, teplo, ktoré sa uvoľňuje do ovzdušia, negatívne, pretože znižuje energiu látky, a práca vrtule, ktorá zvyšovala energiu, sa pozitívne podpísala.
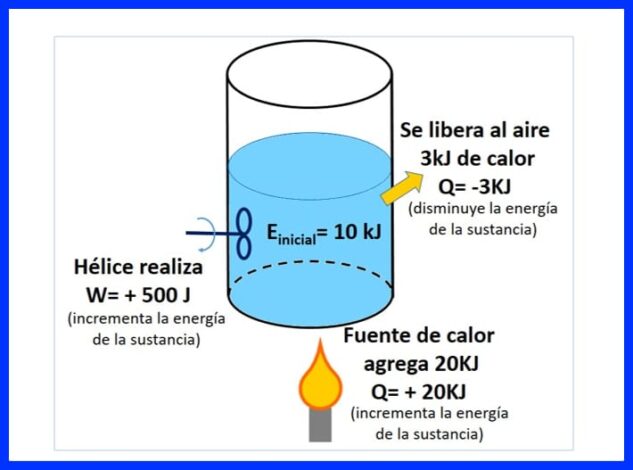
Na obrázku 10 je znázornená energetická bilancia podľa prvého termodynamického zákona a získa sa konečná energia látky.

Druhý zákon termodynamiky
Existuje niekoľko výrokov druhého zákona termodynamiky: Výrok Planck-Kelvina, Clausius, Carnot. Každý z nich ukazuje iný aspekt druhého zákona. Druhý zákon termodynamiky všeobecne predpokladá:
- Smer termodynamických procesov, nezvratnosť fyzikálnych javov.
- Účinnosť tepelných strojov.
- Zadajte vlastnosť „entropia“.
Smer termodynamických procesov:
Spontánne v prírode prúdi energia alebo sa prenáša z najvyššieho energetického stavu do najnižšieho energetického stavu. Teplo prúdi z horúcich telies do chladných telies, a nie naopak. Pozri obrázok 11.

Účinnosť alebo tepelný výkon:
Podľa prvého zákona termodynamiky sa energia ani nevytvára, ani nezničí, ale dá sa transformovať alebo preniesť. Ale pri všetkých prenosoch alebo transformáciách energie nie je množstvo práce užitočné. Pri prenose alebo transformácii energie sa časť počiatočnej energie uvoľňuje ako tepelná energia: energia sa degraduje, stráca kvalitu.
Pri akejkoľvek transformácii energie je množstvo získanej energie vždy menšie ako dodaná energia. Tepelná účinnosť je množstvo tepla zo zdroja, ktoré sa premieňa na prácu, pomer medzi získanou užitočnou energiou a energiou dodanou pri transformácii. Pozri obrázok 12.

Tepelný stroj alebo tepelný stroj:
Tepelný stroj je zariadenie, ktoré čiastočne premieňa teplo na pracovnú alebo mechanickú energiu, vyžaduje k tomu zdroj, ktorý dodáva teplo pri vysokej teplote.
V tepelných strojoch sa používa látka ako vodná para, vzduch alebo palivo. Látka prechádza cyklickým spôsobom radom termodynamických transformácií, aby stroj mohol pracovať nepretržite.
Cvičenie 2.
Motor nákladného vozidla produkuje teplo pri spaľovaní spaľovaním benzínu. Pre každý cyklus motora sa teplo 5 kJ premení na 1kJ mechanickej práce. Aká je účinnosť motora? Koľko tepla sa uvoľní pre každý cyklus motora? Pozri obrázok 13
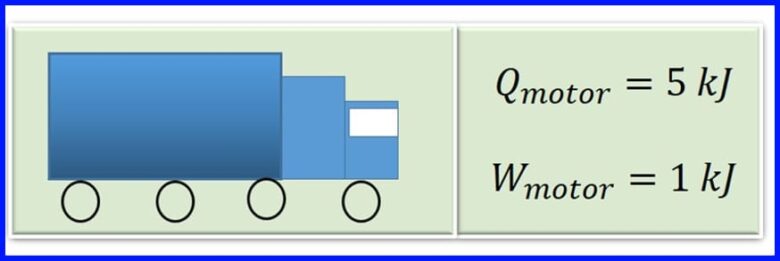
riešenie:

Na určenie uvoľneného tepla sa predpokladá, že v tepelných strojoch sa čistá práca rovná čistému prenosu tepla do systému. Pozri obrázok 14.

Entropia:
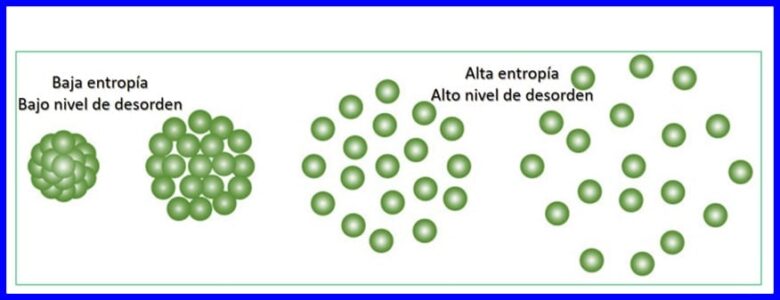
Entropia je miera náhodnosti alebo poruchy v systéme. Entropia umožňuje kvantifikovať časť energie, ktorá sa nedá použiť na výrobu práce, to znamená, že umožňuje kvantifikovať nezvratnosť termodynamického procesu.
Každý prenos energie, ktorý sa vyskytuje, zvyšuje entropiu vesmíru a znižuje množstvo využiteľnej energie dostupnej na prácu. Akýkoľvek termodynamický proces bude prebiehať v smere, ktorý zvyšuje celkovú entropiu vesmíru. Pozri obrázok 15.
3. zákon termodynamiky
Tretí zákon termodynamiky alebo Nerstov postulát
Tretí zákon termodynamiky súvisí s teplotou a chladením. Tvrdí, že entropia systému pri absolútnej nule je určitou konštantou. Pozri obrázok 16.
Absolútna nula je najnižšia teplota, pod ktorou už nie je nižšia miera, je najchladnejšia, akou telo môže byť. Absolútna nula je 0 K, čo zodpovedá –273,15 ° C.

Záver
Existujú štyri termodynamické princípy. Na princípe nula je stanovené, že tepelná rovnováha nastáva, keď majú dve alebo viac telies rovnakú teplotu.
Prvý zákon termodynamiky sa zaoberá zachovaním energie medzi procesmi, zatiaľ čo druhý zákon termodynamiky sa zaoberá smernosťou od najnižšej po najvyššiu entropiu a účinnosťou alebo výkonom tepelných motorov, ktoré premieňajú teplo na prácu.
Tretí zákon termodynamiky súvisí s teplotou a chladením, uvádza sa v ňom, že entropia systému pri absolútnej nule je určitou konštantou.