Principii termodinamice
Pentru a înțelege, într-un mod ușor, lumea largă și complexă a termodinamicii, se recomandă să parcurgeți pas cu pas începând cu o revizuire a termenilor de bază, o introducere în principiile termodinamice și apoi studierea mai aprofundată a legilor termodinamice, modul în care acestea sunt exprimate matematic.și aplicațiile sale.
Cu cele patru legi ale termodinamicii (legea zero, prima lege, a doua lege și a treia lege), este descris modul în care funcționează transferurile și transformările de energie între diferite sisteme; fiind baza pentru înțelegerea multor fenomene fizico-chimice ale naturii.
Revizuirea conceptelor de bază
Vă invităm să vedeți articolul TERMODINAMICA, ce este și aplicațiile sale

Puteți completa aceste informații cu articolul Puterea legii lui Watt (Aplicații - Exerciții) Deocamdată VA URMAM ...
Forme de energie
Energia, proprietatea corpurilor de a se transforma prin modificarea situației sau stării lor, vine sub multe forme, cum ar fi energia cinetică, energia potențială și energia internă a corpurilor. Vezi figura 1.
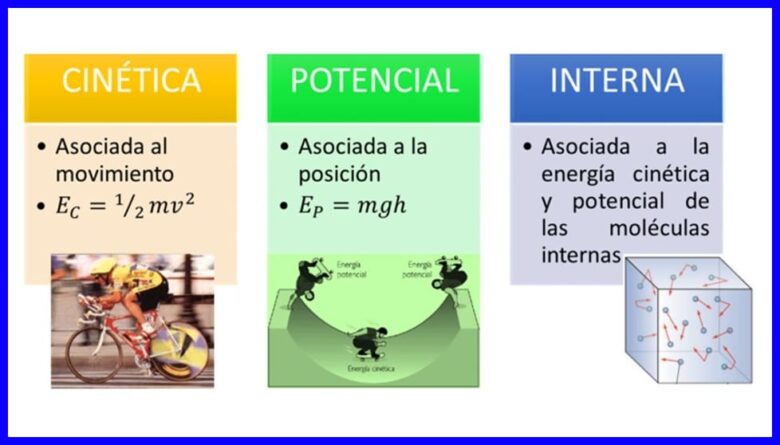
Muncă
Este produsul unei forțe și al unei deplasări, ambele măsurate în aceeași direcție. Pentru a calcula lucrarea, se folosește componenta forței care este paralelă cu deplasarea obiectului. Lucrul se măsoară în Nm, Joule (J), ft.lb-f sau BTU. Vezi figura 2.
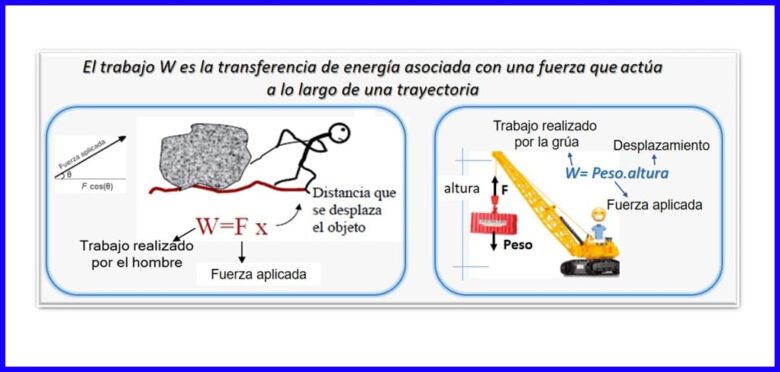
Căldură (Q)
Transferul de energie termică între două corpuri care se află la temperaturi diferite și are loc doar în sensul că temperatura scade. Căldura se măsoară în Joule, BTU, lire-picioare sau în calorii. Vezi figura 3.
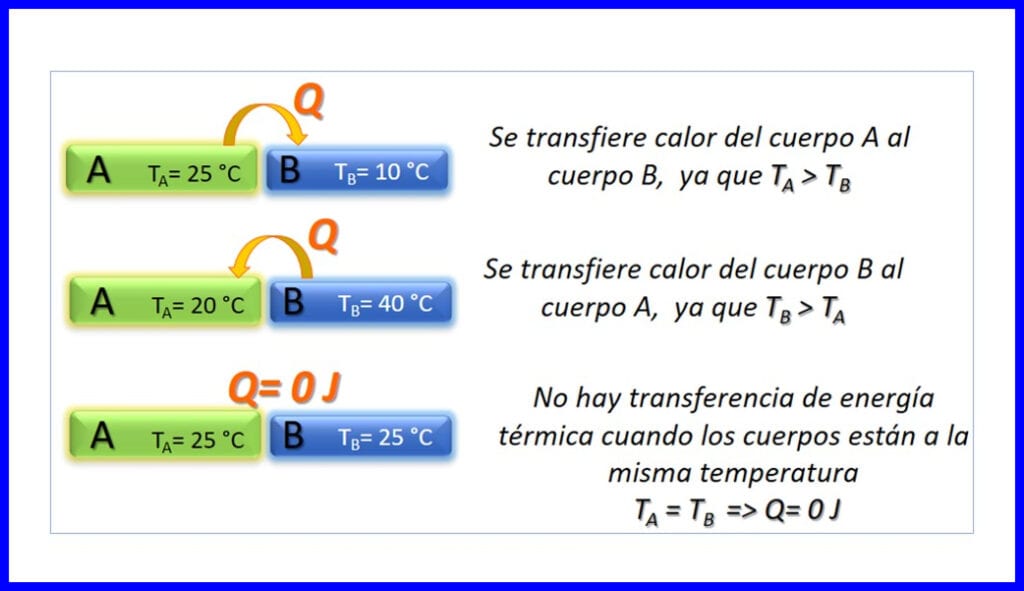
Principii termodinamice
Legea zero - Principiul zero
Legea zero a termodinamicii afirmă că dacă două obiecte, A și B, sunt în echilibru termic între ele, iar obiectul A este în echilibru cu un al treilea obiect C, atunci obiectul B se află în echilibru termic cu obiectul C. Echilibrul termic are loc când două sau mai multe corpuri sunt la aceeași temperatură. Vezi figura 4.
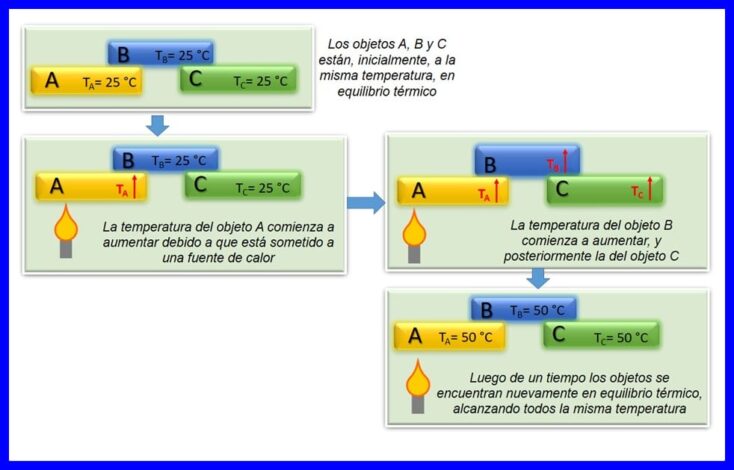
Această lege este considerată o lege de bază a termodinamicii. A fost postulat ca „Legea zero” în 1935, deoarece a fost postulat după ce au fost făcute prima și a doua legi ale termodinamicii.
Prima lege a termodinamicii (principiul conservării energiei)
Declarația primei legi a termodinamicii:
Prima lege a termodinamicii, cunoscută și sub numele de principiul conservării energiei, afirmă că energia nu este creată sau distrusă, este transformată doar într-un alt tip de energie sau este transferată de la un obiect la altul. Astfel, cantitatea totală de energie din univers nu se schimbă.
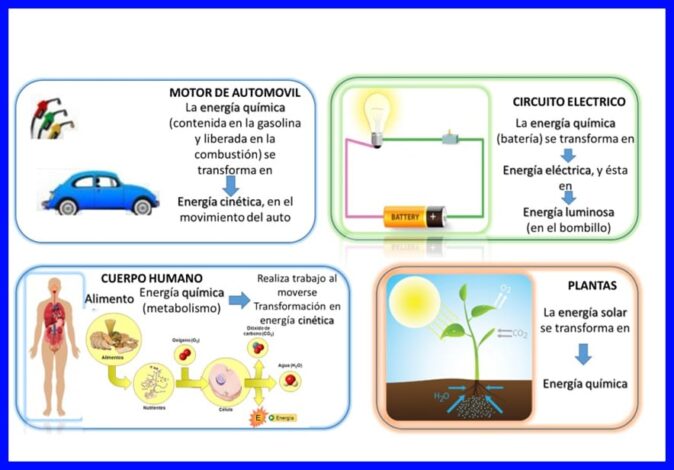
Prima lege este îndeplinită în „totul”, energia este transferată și transformată continuu, de exemplu, în unele dispozitive electrice, cum ar fi mixere și mixere, energia electrică este transformată în energie mecanică și termică, în corpul uman sunt transformate substanța chimică energia alimentelor care este ingerată în energia cinetică atunci când corpul este în mișcare sau alte exemple precum cele prezentate în figura 5.
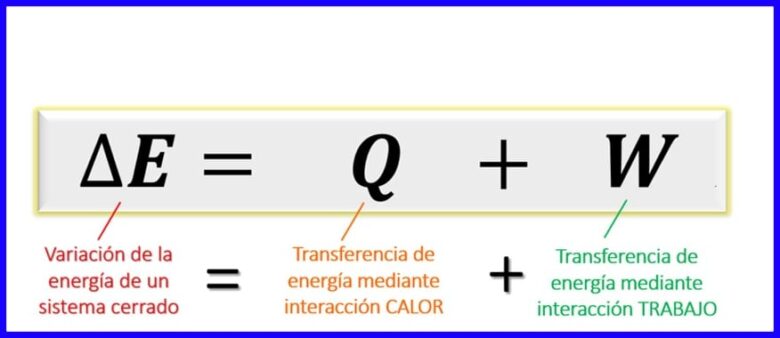
Ecuația primei legi a termodinamicii:
Ecuația primei legi din cadrul principiilor termodinamice exprimă echilibrul care trebuie să existe între diferitele tipuri de energie într-un proces dat. Deoarece, în sistemele închise [1], schimburile de energie pot fi date numai prin transferul de căldură sau prin munca efectuată (de către sau pe sistem) se stabilește că variația de energie a unui sistem este egală cu suma transferurile de energie prin căldură și prin muncă. Vezi figura 6.
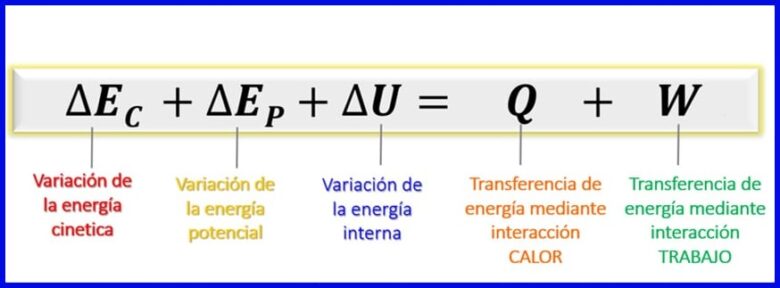
Având în vedere că energiile luate în considerare în acest bilanț energetic sunt energia cinetică, energia potențială și energia internă [1], bilanțul energetic pentru sistemele închise rămâne așa cum se arată în figura 7.
- (ec) Energie kinetică , datorită mișcării unui corp;
- (ep) Energie potențială, datorită poziției unui corp într-un câmp gravitațional;
- (SAU) Energie interna , datorită contribuțiilor microscopice ale energiei cinetice și potențiale a moleculelor interne ale unui corp.
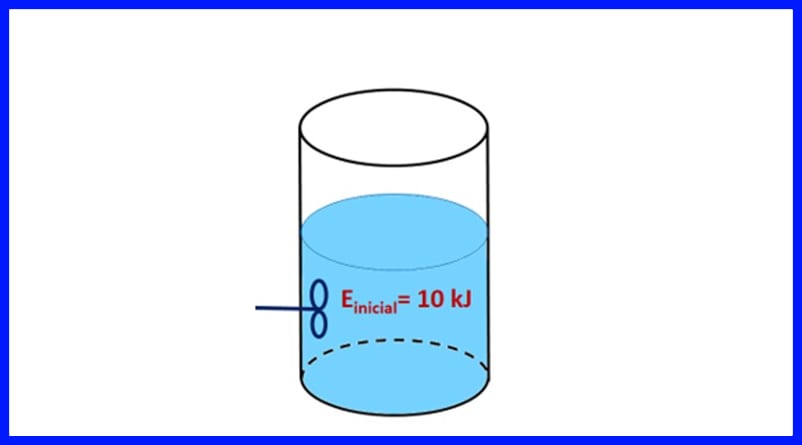
Exercițiul 1.
Un recipient sigilat conține o substanță, cu o energie inițială de 10 kJ. Substanța este agitată cu o elice care funcționează cu 500 J, în timp ce o sursă de căldură transferă 20 kJ de căldură substanței. În plus, 3kJ de căldură este eliberată în aer în timpul procesului. Determinați energia finală a substanței. Vezi figura 8.
Soluţie:
În figura 9 puteți vedea căldura adăugată de sursa de căldură, care este considerată „pozitivă”, deoarece crește energia substanței, căldura care este eliberată în aer, negativă, deoarece scade energia substanței și lucrarea elicei, care a crescut energia a luat un semn pozitiv.
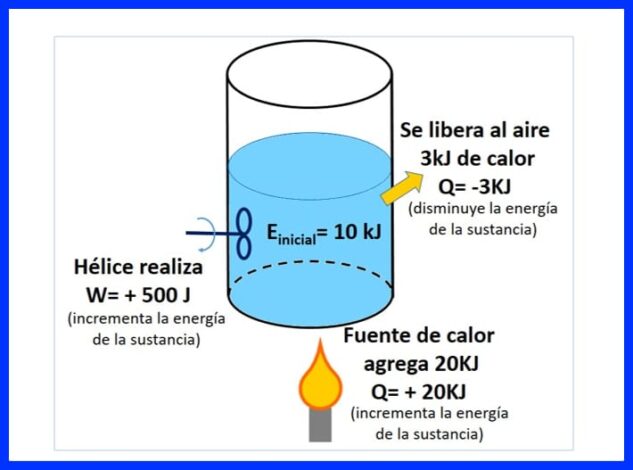
În figura 10 este prezentat bilanțul energetic, conform primei legi a termodinamicii și se obține energia finală a substanței.

A doua lege a termodinamicii
Există mai multe afirmații ale celei de-a doua legi a termodinamicii: Afirmația lui Planck-Kelvin, Clausius, Carnot. Fiecare dintre ele prezintă un aspect diferit al celei de-a doua legi. În general, a doua lege a termodinamicii postulează:
- Direcția proceselor termodinamice, ireversibilitatea fenomenelor fizice.
- Eficiența mașinilor termice.
- Introduceți proprietatea „entropie”.
Direcția proceselor termodinamice:
Spontan, în natură, energia curge sau este transferată de la cea mai înaltă stare energetică la cea mai scăzută stare energetică. Căldura curge de la corpuri fierbinți la corpuri reci și nu invers. Vezi figura 11.

Eficiență sau performanță termică:
Conform primei legi a termodinamicii, energia nu este nici creată, nici distrusă, dar poate fi transformată sau transferată. Dar în toate transferurile sau transformările de energie, o cantitate din aceasta nu este utilă pentru a lucra. Pe măsură ce energia este transferată sau transformată, o parte din energia inițială este eliberată ca energie termică: energia se degradează, își pierde calitatea.
În orice transformare a energiei, cantitatea de energie obținută este întotdeauna mai mică decât energia furnizată. Eficiența termică este cantitatea de căldură din sursa care este transformată în muncă, raportul dintre energia utilă obținută și energia furnizată într-o transformare. Vezi figura 12.

Mașină termică sau mașină termică:
Mașina termică este un dispozitiv care transformă parțial căldura în muncă sau energie mecanică, pentru care necesită o sursă care furnizează căldură la temperatură ridicată.
La mașinile termice se folosește o substanță precum vapori de apă, aer sau combustibil. Substanța suferă o serie de transformări termodinamice într-un mod ciclic, astfel încât mașina să poată funcționa continuu.
Exercițiul 2.
Motorul unui vehicul de marfă produce căldură în combustie prin arderea benzinei. Pentru fiecare ciclu al motorului, căldura de 5 kJ este transformată în 1kJ de lucru mecanic. Care este eficiența motorului? Câtă căldură este eliberată pentru fiecare ciclu al motorului? Vezi figura 13
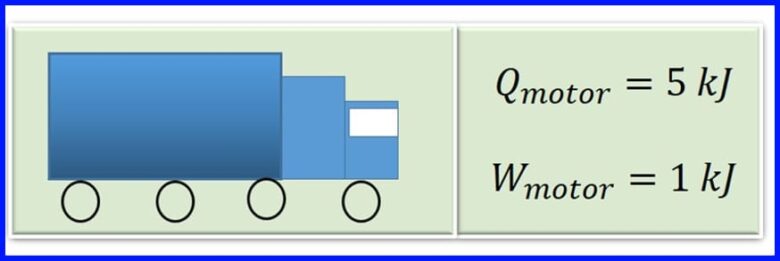
Soluţie:

Pentru a determina căldura degajată, se presupune că la mașinile termice, lucrul net este egal cu transferul net de căldură către sistem. Vezi figura 14.

Entropie:
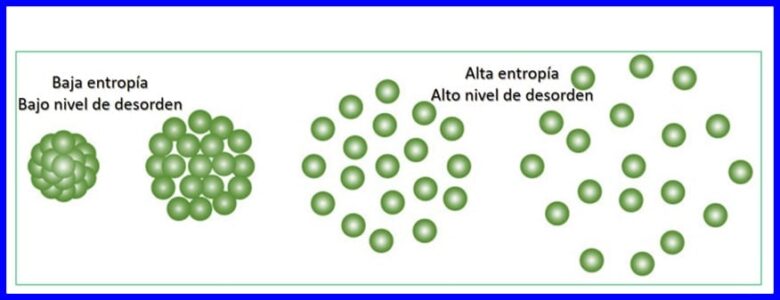
Entropia este gradul de întâmplare sau tulburare dintr-un sistem. Entropia face posibilă cuantificarea părții de energie care nu poate fi utilizată pentru a produce muncă, adică face posibilă cuantificarea ireversibilității unui proces termodinamic.
Fiecare transfer de energie care are loc crește entropia universului și reduce cantitatea de energie utilizabilă disponibilă pentru a lucra. Orice proces termodinamic va continua într-o direcție care crește entropia totală a universului. Vezi figura 15.
A treia lege a termodinamicii
A treia lege a termodinamicii sau postulat Nerst
A treia lege a termodinamicii este legată de temperatură și răcire. Se afirmă că entropia unui sistem la zero absolut este o constantă definită. Vezi figura 16.
Zero absolut este cea mai scăzută temperatură sub care nu mai există o măsură mai mică, este cea mai rece care poate fi un corp. Zero absolut este 0 K, echivalent cu -273,15 ºC.

Concluzie
Există patru principii termodinamice. În principiul zero se stabilește că echilibrul termic apare atunci când două sau mai multe corpuri sunt la aceeași temperatură.
Prima lege a termodinamicii se referă la conservarea energiei între procese, în timp ce a doua lege a termodinamicii se referă la direcționalitatea de la cea mai mică la cea mai mare entropie și eficiența sau performanța motoarelor termice care transformă căldura în lucru.
A treia lege a termodinamicii este legată de temperatură și răcire, afirmă că entropia unui sistem la zero absolut este o constantă definitivă.