Thermodynamische principes
Om de wijde en complexe wereld van de thermodynamica op een gemakkelijke manier te begrijpen, wordt aanbevolen om stap voor stap te beginnen met een overzicht van de basistermen, een inleiding tot thermodynamische principes en vervolgens dieper de thermodynamische wetten te bestuderen, hoe ze worden wiskundig uitgedrukt. en zijn toepassingen.
Met de vier wetten van de thermodynamica (nulwet, eerste wet, tweede wet en derde wet), wordt beschreven hoe de overdrachten en transformaties van energie tussen verschillende systemen werken; de basis vormen voor het begrijpen van vele fysisch-chemische verschijnselen van de natuur.
Herziening van basisconcepten
We nodigen je uit om het artikel te zien THERMODYNAMICA, wat het is en de toepassingen

U kunt deze informatie aanvullen met het artikel De kracht van de wet van Watt (toepassingen - oefeningen) Voorlopig WIJ VOLGEN ...
Vormen van energie
Energie, de eigenschap van lichamen om zichzelf te transformeren door hun situatie of toestand aan te passen, komt in vele vormen voor, zoals kinetische energie, potentiële energie en interne energie van lichamen. Zie figuur 1.
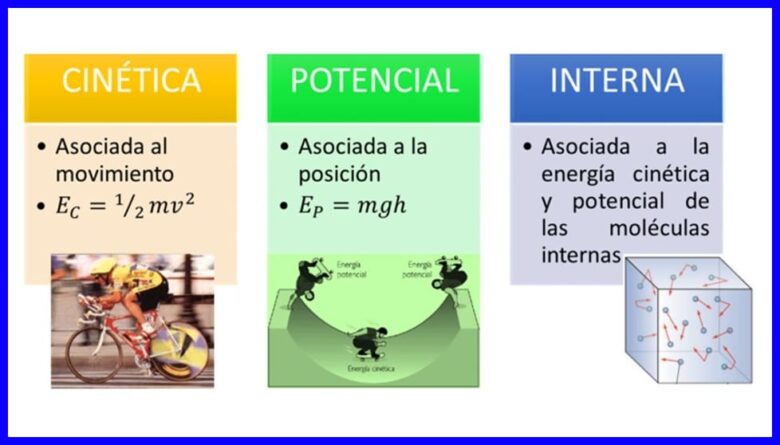
Werken
Het is het product van een kracht en verplaatsing, beide gemeten in dezelfde richting. Om het werk te berekenen, wordt de component van de kracht gebruikt die parallel is aan de verplaatsing van het object. Werk wordt gemeten in Nm, Joule (J), ft.lb-f of BTU. Zie figuur 2.
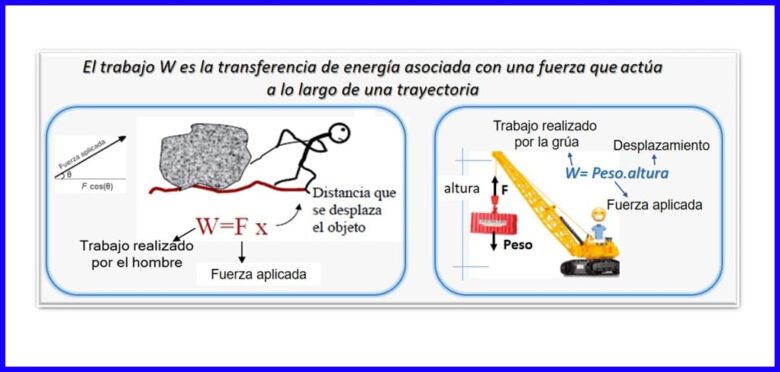
Warmte (Q)
Overdracht van thermische energie tussen twee lichamen met verschillende temperaturen, en het vindt alleen plaats in de zin dat de temperatuur afneemt. Warmte wordt gemeten in joule, BTU, pond-voet of in calorieën. Zie figuur 3.
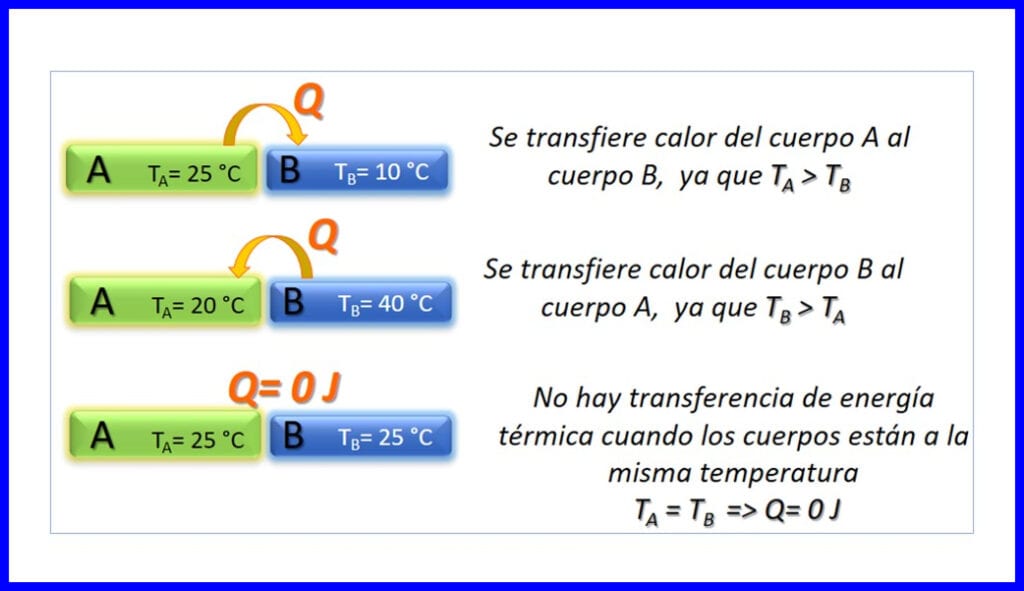
Thermodynamische principes
Zero Law - Zero Principle
De nulwet van de thermodynamica stelt dat als twee objecten, A en B, in thermisch evenwicht met elkaar zijn en object A in evenwicht is met een derde object C, object B in thermisch evenwicht is met object C.Het thermisch evenwicht treedt op wanneer twee of meer lichamen dezelfde temperatuur hebben. Zie figuur 4.
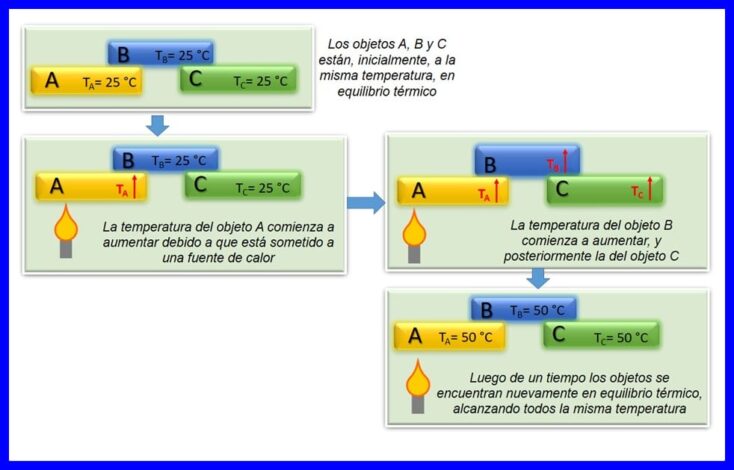
Deze wet wordt beschouwd als een basiswet van de thermodynamica. Het werd gepostuleerd als "nulwet", in 1935, aangezien het werd gepostuleerd nadat de eerste en tweede wetten van de thermodynamica waren gemaakt.
1e wet van de thermodynamica (principe van energiebehoud)
Verklaring van de eerste wet van de thermodynamica:
De eerste wet van de thermodynamica, ook wel het principe van behoud van energie genoemd, stelt dat energie niet wordt gecreëerd of vernietigd, maar alleen wordt omgezet in een ander type energie, of dat het van het ene object naar het andere wordt overgebracht. De totale hoeveelheid energie in het universum verandert dus niet.
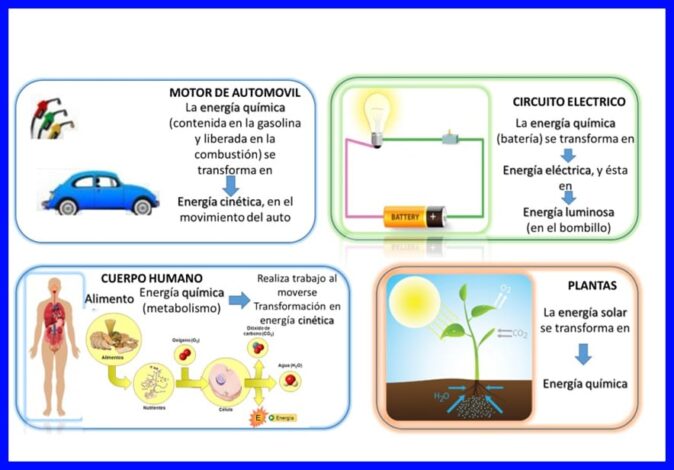
De eerste wet wordt vervuld in "alles", energie wordt continu overgedragen en getransformeerd, bijvoorbeeld in sommige elektrische apparaten, zoals mixers en blenders, wordt elektrische energie omgezet in mechanische en thermische energie, in het menselijk lichaam worden ze omgezet in de chemische stof energie van voedsel dat wordt opgenomen in kinetische energie wanneer het lichaam in beweging is, of andere voorbeelden zoals getoond in figuur 5.
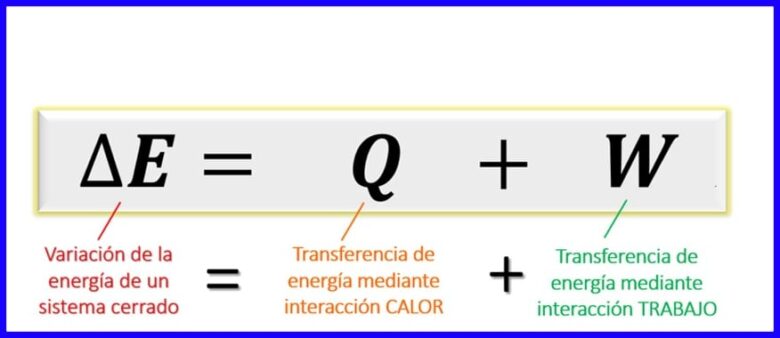
Vergelijking van de eerste wet van de thermodynamica:
De vergelijking van de eerste wet binnen de thermodynamische principes drukt het evenwicht uit dat moet bestaan tussen de verschillende soorten energie in een bepaald proces. Omdat in gesloten systemen [1] de energie-uitwisselingen alleen kunnen plaatsvinden door warmteoverdracht of door het werk (door of aan het systeem) wordt vastgesteld dat de energievariatie van een systeem gelijk is aan de som van energieoverdracht door warmte en door werk. Zie figuur 6.
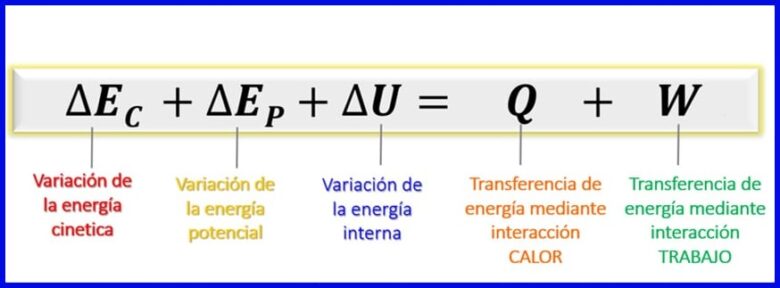
Aangezien de energieën die in deze energiebalans in aanmerking worden genomen, kinetische energie, potentiële energie en interne energie [1] zijn, blijft de energiebalans voor gesloten systemen zoals weergegeven in figuur 7.
- (bv) Kinetische energie , door de beweging van een lichaam;
- (ep) Potentiële energie, vanwege de positie van een lichaam in een zwaartekrachtveld;
- (OF) Interne energie , vanwege de microscopische bijdragen van de kinetische en potentiële energie van de interne moleculen van een lichaam.
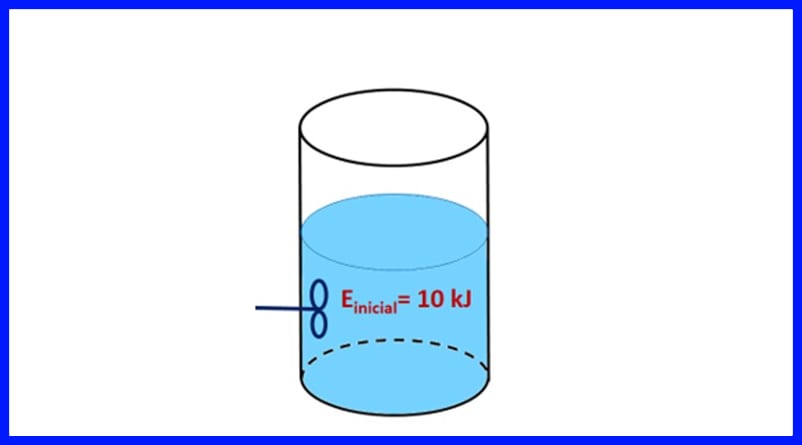
Oefening 1.
Een verzegelde container bevat een stof, met een aanvankelijke energie van 10 kJ. De substantie wordt geroerd met een propeller die 500 J werk doet, terwijl een warmtebron 20 kJ warmte aan de substantie overbrengt. Bovendien wordt tijdens het proces 3 kJ warmte in de lucht afgegeven. Bepaal de uiteindelijke energie van de stof. Zie figuur 8.
Oplossing:
In figuur 9 kun je de warmte zien die wordt toegevoegd door de warmtebron, die als 'positief' wordt beschouwd omdat het de energie van de stof verhoogt, de warmte die vrijkomt in de lucht, negatief omdat het de energie van de stof verlaagt, en de werk van de propeller, die de energie verhoogde, nam een positief teken aan.
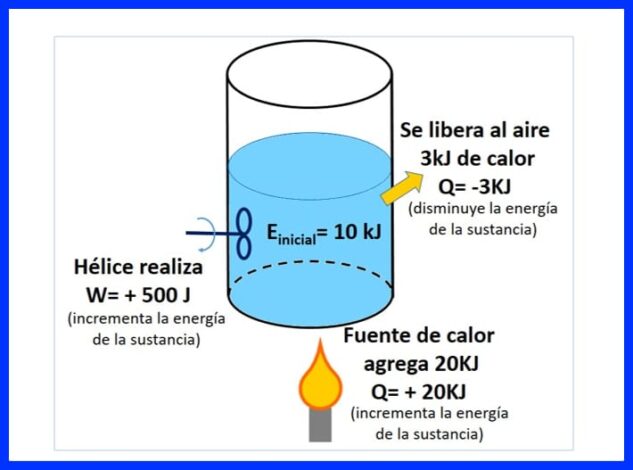
In figuur 10 wordt de energiebalans weergegeven volgens de eerste wet van de thermodynamica en wordt de eindenergie van de stof verkregen.

Tweede wet van de thermodynamica
Er zijn verschillende uitspraken van de tweede wet van de thermodynamica: Statement of Planck-Kelvin, Clausius, Carnot. Elk van hen toont een ander aspect van de tweede wet. In het algemeen postuleert de tweede wet van de thermodynamica:
- De richting van thermodynamische processen, onomkeerbaarheid van fysische verschijnselen.
- De efficiëntie van thermische machines.
- Voer de eigenschap "entropy" in.
Richting van thermodynamische processen:
In de natuur stroomt of wordt energie spontaan overgebracht van de hoogste energietoestand naar de laagste energietoestand. Warmte stroomt van hete lichamen naar koude lichamen en niet andersom. Zie figuur 11.

Efficiëntie of thermische prestaties:
Volgens de eerste wet van de thermodynamica wordt energie niet gecreëerd of vernietigd, maar kan het worden getransformeerd of overgedragen. Maar bij alle energieoverdrachten of -transformaties is een deel ervan niet zinvol om werk te doen. Terwijl energie wordt overgedragen of omgezet, komt een deel van de aanvankelijke energie vrij als thermische energie: energie degradeert, verliest kwaliteit.
Bij elke energietransformatie is de hoeveelheid verkregen energie altijd minder dan de geleverde energie. Thermisch rendement is de hoeveelheid warmte van de bron die wordt omgezet in arbeid, de verhouding tussen de verkregen nuttige energie en de energie die bij een transformatie wordt geleverd. Zie figuur 12.

Thermische machine of hittemachine:
De thermische machine is een apparaat dat warmte gedeeltelijk omzet in arbeid of mechanische energie, waarvoor het een bron nodig heeft die warmte op hoge temperatuur levert.
In thermische machines wordt een stof zoals waterdamp, lucht of brandstof gebruikt. De stof ondergaat op cyclische wijze een reeks thermodynamische transformaties, zodat de machine continu kan draaien.
Oefening 2.
De motor van een vrachtvoertuig produceert warmte bij verbranding door benzine te verbranden. Voor elke cyclus van de motor wordt de warmte van 5 kJ omgezet in 1 kJ mechanisch werk. Wat is de efficiëntie van de motor? Hoeveel warmte komt er vrij voor elke cyclus van de motor? Zie figuur 13
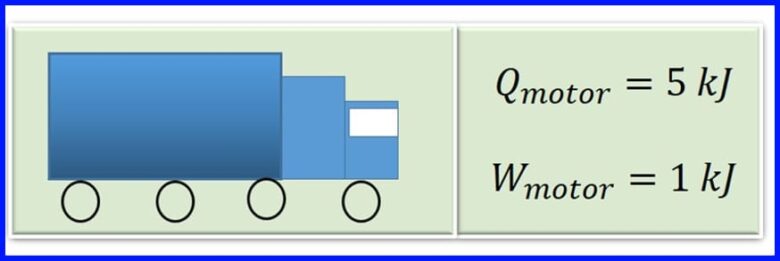
Oplossing:

Om de vrijkomende warmte te bepalen, wordt aangenomen dat bij thermische machines het netto werk gelijk is aan de netto warmteoverdracht naar het systeem. Zie figuur 14.

Entropie:
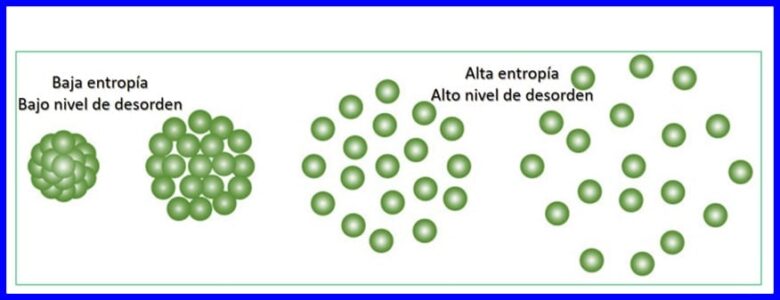
Entropie is de mate van willekeur of wanorde in een systeem. Entropie maakt het mogelijk om het deel van de energie te kwantificeren dat niet kan worden gebruikt om werk te produceren, dat wil zeggen, het maakt het mogelijk om de onomkeerbaarheid van een thermodynamisch proces te kwantificeren.
Elke energieoverdracht die plaatsvindt, verhoogt de entropie van het universum en vermindert de hoeveelheid bruikbare energie die beschikbaar is om werk te doen. Elk thermodynamisch proces zal zich voortzetten in een richting die de totale entropie van het universum vergroot. Zie figuur 15.
3e wet van de thermodynamica
Derde wet van de thermodynamica of Nerst-postulaat
De derde wet van de thermodynamica heeft betrekking op temperatuur en koeling. Het stelt dat de entropie van een systeem op het absolute nulpunt een welomlijnde constante is. Zie figuur 16.
Het absolute nulpunt is de laagste temperatuur waaronder er geen lagere maat meer is, het is de koudste die een lichaam kan zijn. Het absolute nulpunt is 0 K, wat overeenkomt met -273,15 ºC.

Conclusie
Er zijn vier thermodynamische principes. In het nulprincipe wordt vastgesteld dat thermisch evenwicht optreedt wanneer twee of meer lichamen dezelfde temperatuur hebben.
De eerste wet van de thermodynamica behandelt het behoud van energie tussen processen, terwijl de tweede wet van de thermodynamica zich bezighoudt met de directionaliteit van de laagste naar de hoogste entropie, en de efficiëntie of prestaties van warmtemotoren die warmte omzetten in werk.
De derde wet van de thermodynamica heeft betrekking op temperatuur en koeling, het stelt dat de entropie van een systeem op het absolute nulpunt een welomlijnde constante is.