थर्मोडायनामिक सिद्धांत
समझने के लिए, एक आसान तरीके से, थर्मोडायनामिक्स की विस्तृत और जटिल दुनिया में, मूल शब्दों की समीक्षा, थर्मोडायनामिक सिद्धांतों का परिचय, और फिर अधिक गहराई से थर्मोडायनामिक कानूनों का अध्ययन करते हुए, कदम से कदम पर जाने की सिफारिश की जाती है कि वे कैसे गणितीय रूप से व्यक्त किए गए हैं और इसके अनुप्रयोग।
ऊष्मप्रवैगिकी के चार कानूनों (शून्य कानून, पहला कानून, दूसरा कानून और तीसरा कानून) के साथ, यह वर्णित है कि विभिन्न प्रणालियों के बीच ऊर्जा के हस्तांतरण और परिवर्तन कैसे काम करते हैं; प्रकृति की कई भौतिक रासायनिक घटनाओं को समझने का आधार है।
बुनियादी अवधारणाओं की समीक्षा
हम आपको लेख देखने के लिए आमंत्रित करते हैं THERMODYNAMICS, यह क्या है और इसके अनुप्रयोग

आप इस जानकारी को लेख के साथ पूरक कर सकते हैं वाट की विधि की शक्ति (अनुप्रयोग - अभ्यास) कुछ समय के लिए हम फ़ॉलो करते हैं ...
ऊर्जा के रूप
ऊर्जा, अपनी स्थिति या स्थिति को संशोधित करके खुद को बदलने के लिए निकायों की संपत्ति, कई रूपों में होती है, जैसे कि गतिज ऊर्जा, संभावित ऊर्जा और निकायों की आंतरिक ऊर्जा। आकृति 1 देखें।
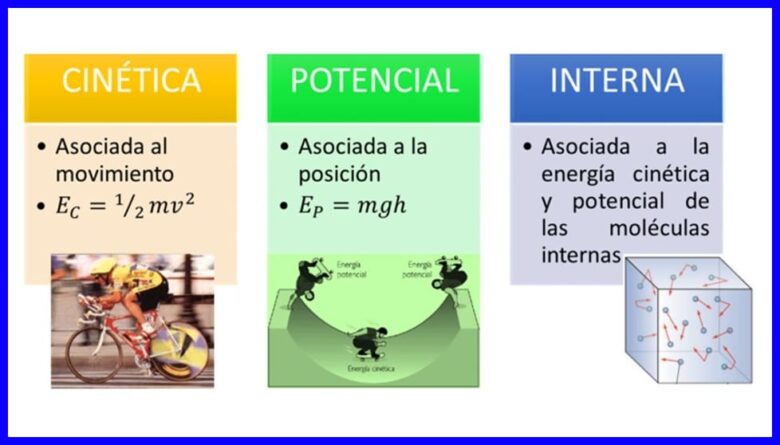
काम
यह एक बल और विस्थापन का उत्पाद है, दोनों को एक ही दिशा में मापा जाता है। कार्य की गणना करने के लिए, वस्तु के विस्थापन के समानांतर बल के घटक का उपयोग किया जाता है। कार्य Nm, Joule (J), ft.lb-f, या BTU में मापा जाता है। आकृति 2 देखें।
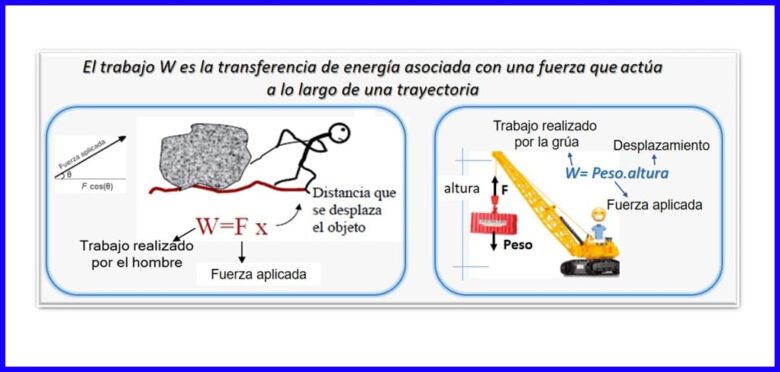
हीट (Q)
दो निकायों के बीच थर्मल ऊर्जा का स्थानांतरण जो विभिन्न तापमानों पर होता है, और यह केवल इस अर्थ में होता है कि तापमान कम हो जाता है। हीट को जूल, बीटीयू, पाउंड-फीट या कैलोरी में मापा जाता है। आकृति 3 देखें।
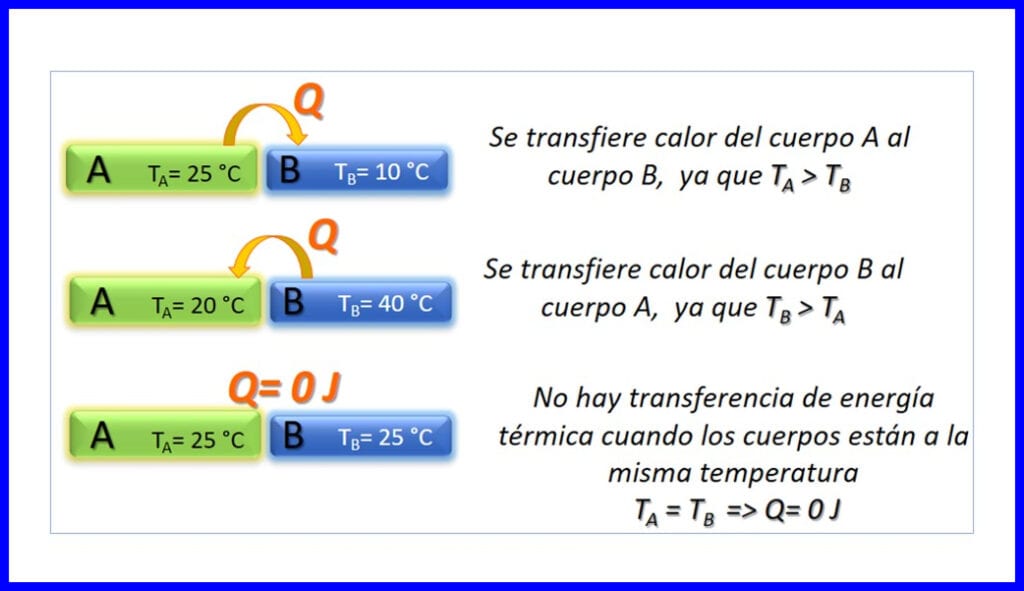
थर्मोडायनामिक सिद्धांत
शून्य कानून - शून्य सिद्धांत
ऊष्मा गतिकी का शून्य नियम बताता है कि यदि दो वस्तुएं, A और B, एक दूसरे के साथ थर्मल संतुलन में हैं, और ऑब्जेक्ट A एक तीसरी वस्तु C के साथ संतुलन में है, तो वस्तु B, C के साथ थर्मल संतुलन में है। थर्मल संतुलन होता है जब दो या दो से अधिक शरीर एक ही तापमान पर हों। आकृति 4 देखें।
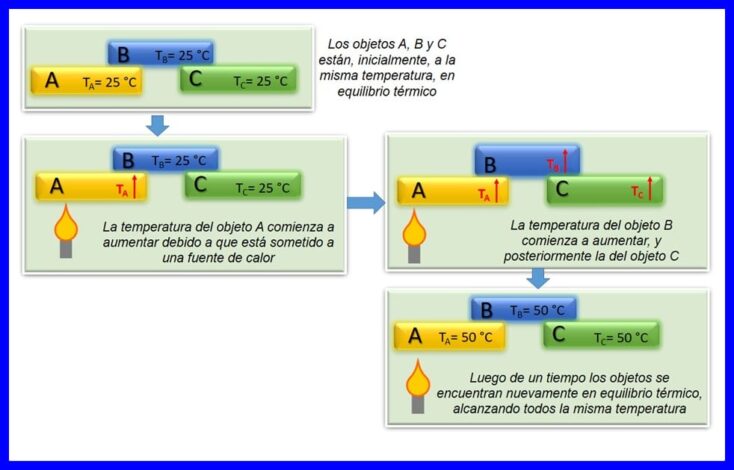
इस कानून को उष्मागतिकी का एक बुनियादी नियम माना जाता है। 1935 में इसे "शून्य कानून" के रूप में पोस्ट किया गया था, क्योंकि इसे थर्मोडायनामिक्स के पहले और दूसरे कानून के बाद पोस्ट किया गया था।
1 ऊष्मप्रवैगिकी कानून (ऊर्जा संरक्षण का सिद्धांत)
ऊष्मप्रवैगिकी के पहले कानून का विवरण:
ऊष्मप्रवैगिकी का पहला नियम, जिसे ऊर्जा के संरक्षण के सिद्धांत के रूप में भी जाना जाता है, कहता है कि ऊर्जा का निर्माण या विनाश नहीं होता है, यह केवल दूसरे प्रकार की ऊर्जा में परिवर्तित होता है, या इसे एक वस्तु से दूसरी वस्तु में स्थानांतरित किया जाता है। इस प्रकार ब्रह्मांड में ऊर्जा की कुल मात्रा नहीं बदलती है।
पहला कानून "सब कुछ" में पूरा होता है, ऊर्जा को स्थानांतरित और लगातार रूपांतरित किया जाता है, उदाहरण के लिए, कुछ विद्युत उपकरणों में, जैसे मिक्सर और मिक्सर, विद्युत ऊर्जा को यांत्रिक और थर्मल ऊर्जा में बदल दिया जाता है, मानव शरीर में वे रासायनिक रूपांतरित होते हैं भोजन की ऊर्जा, जो शरीर में गति होने पर गतिज ऊर्जा में लिप्त होती है, या अन्य उदाहरण जैसे कि आकृति 5 में दिखाए गए हैं।
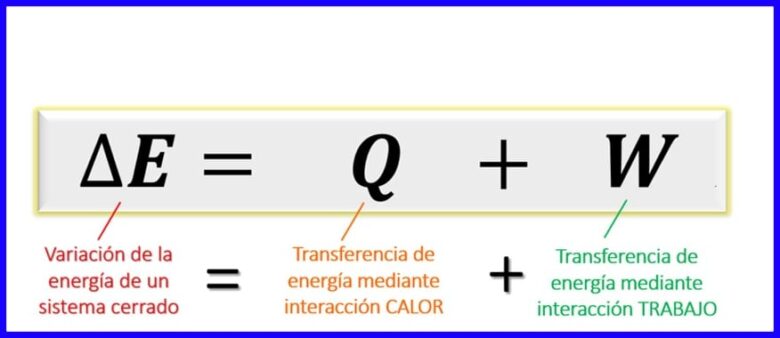
ऊष्मप्रवैगिकी के पहले कानून का समीकरण:
थर्मोडायनामिक सिद्धांतों के भीतर पहले कानून का समीकरण उस संतुलन को व्यक्त करता है जो किसी दिए गए प्रक्रिया में विभिन्न प्रकार की ऊर्जा के बीच मौजूद होना चाहिए। चूंकि, बंद सिस्टम [1] में, ऊर्जा का आदान-प्रदान केवल गर्मी के हस्तांतरण द्वारा किया जा सकता है, या काम के द्वारा (सिस्टम पर या) द्वारा किया जाता है, यह स्थापित किया जाता है कि सिस्टम की ऊर्जा भिन्नता राशि के योग के बराबर है ऊर्जा गर्मी और काम के माध्यम से स्थानांतरित होती है। आकृति 6 देखें।
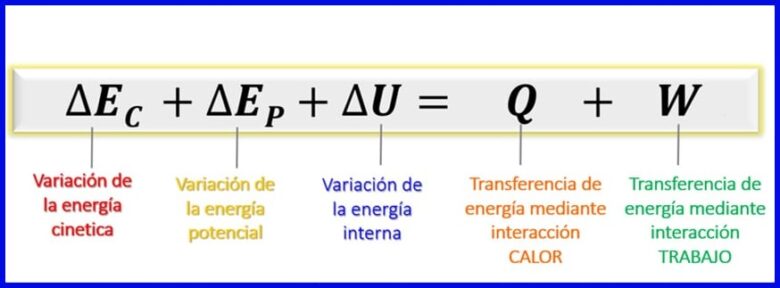
यह देखते हुए कि इस ऊर्जा संतुलन में माना जाने वाला ऊर्जा गतिज ऊर्जा, संभावित ऊर्जा और आंतरिक ऊर्जा है [1], बंद प्रणालियों के लिए ऊर्जा संतुलन जैसा कि आंकड़ा 7 में दिखाया गया है।
- (ईसी) गतिज ऊर्जा , एक शरीर के आंदोलन के कारण;
- (एप) संभावित ऊर्जा, एक गुरुत्वाकर्षण क्षेत्र में एक शरीर की स्थिति के कारण;
- (यू) आंतरिक ऊर्जा , शरीर के आंतरिक अणुओं के गतिज और संभावित ऊर्जा के सूक्ष्म योगदान के कारण।
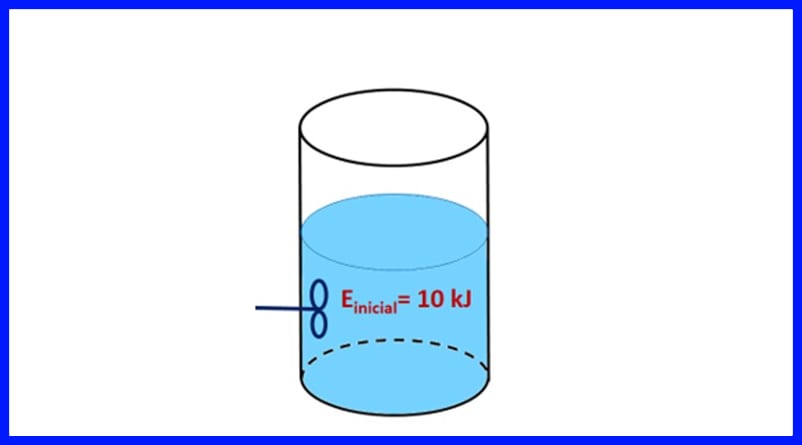
व्यायाम २।
एक सील कंटेनर में 10 केजे की प्रारंभिक ऊर्जा के साथ एक पदार्थ होता है। पदार्थ को एक प्रोपेलर से हिलाया जाता है जो 500 J काम करता है, जबकि एक ऊष्मा स्रोत 20 kJ ऊष्मा को पदार्थ में स्थानांतरित करता है। इसके अलावा, प्रक्रिया के दौरान गर्मी का 3kJ हवा में छोड़ दिया जाता है। पदार्थ की अंतिम ऊर्जा का निर्धारण करें। आकृति 8 देखें।
समाधान:
आंकड़ा 9 में हम ऊष्मा स्रोत द्वारा जोड़े गए ताप को देख सकते हैं, जिसे "सकारात्मक" माना जाता है क्योंकि यह पदार्थ की ऊर्जा को बढ़ाता है, हवा में छोड़ी जाने वाली ऊष्मा, नकारात्मक होती है क्योंकि यह पदार्थ की ऊर्जा को कम करती है, और प्रोपेलर का काम, जिसने ऊर्जा में वृद्धि की, एक सकारात्मक संकेत लिया।
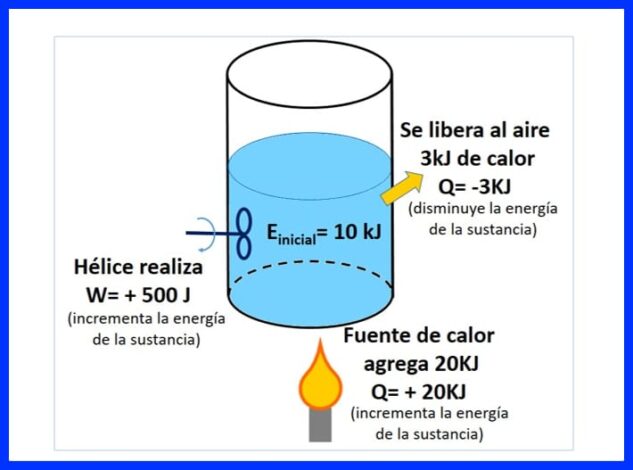
आकृति 10 में ऊष्मा गतिकी का पहला नियम और पदार्थ की अंतिम ऊर्जा के अनुसार ऊर्जा संतुलन प्रस्तुत किया गया है।

उष्मागतिकी का दूसरा नियम
उष्मागतिकी के दूसरे नियम के कई कथन हैं: प्लांक-केल्विन, क्लॉजियस, कारनोट का कथन। उनमें से प्रत्येक दूसरे कानून के एक अलग पहलू को दर्शाता है। सामान्य तौर पर ऊष्मप्रवैगिकी का दूसरा नियम है:
- थर्मोडायनामिक प्रक्रियाओं की दिशा, भौतिक घटना की अपरिवर्तनीयता।
- थर्मल मशीनों की दक्षता।
- संपत्ति "एन्ट्रॉपी" दर्ज करें।
थर्मोडायनामिक प्रक्रियाओं की दिशा:
प्रकृति में सहज रूप से, ऊर्जा प्रवाह या उच्चतम ऊर्जा राज्य से निम्नतम ऊर्जा राज्य में स्थानांतरित किया जाता है। ऊष्मा गर्म पिंडों से ठंडे पिंडों तक जाती है और इसके विपरीत नहीं। आकृति 11 देखें।

दक्षता या थर्मल प्रदर्शन:
ऊष्मप्रवैगिकी के पहले नियम के अनुसार, ऊर्जा न तो बनाई जाती है और न ही नष्ट होती है, लेकिन इसे परिवर्तित या स्थानांतरित किया जा सकता है। लेकिन सभी ऊर्जा हस्तांतरण या परिवर्तनों में इसकी एक मात्रा काम करने के लिए उपयोगी नहीं है। जैसा कि ऊर्जा को स्थानांतरित या परिवर्तित किया जाता है, प्रारंभिक ऊर्जा का हिस्सा थर्मल ऊर्जा के रूप में जारी किया जाता है: ऊर्जा का क्षरण, गुणवत्ता खो देता है।
किसी भी ऊर्जा परिवर्तन में, प्राप्त ऊर्जा की मात्रा हमेशा आपूर्ति की गई ऊर्जा से कम होती है। थर्मल दक्षता उस स्रोत से गर्मी की मात्रा है जिसे काम में परिवर्तित किया जाता है, प्राप्त ऊर्जा के बीच का अनुपात और एक परिवर्तन में आपूर्ति की गई ऊर्जा। आकृति 12 देखें।

थर्मल मशीन या हीट मशीन:
ऊष्मा इंजन एक ऐसा उपकरण है जो आंशिक रूप से ऊष्मा को काम या यांत्रिक ऊर्जा में परिवर्तित करता है, जिसके लिए उसे एक ऐसे स्रोत की आवश्यकता होती है जो उच्च तापमान पर ऊष्मा की आपूर्ति करता है।
थर्मल मशीनों में जल वाष्प, वायु या ईंधन जैसे पदार्थ का उपयोग किया जाता है। पदार्थ एक चक्रीय तरीके से थर्मोडायनामिक परिवर्तनों की एक श्रृंखला से गुजरता है, ताकि मशीन लगातार काम कर सके।
व्यायाम २।
एक कार्गो वाहन का इंजन गैसोलीन को जलाकर दहन में गर्मी पैदा करता है। इंजन के प्रत्येक चक्र के लिए, 5 kJ की ऊष्मा को यांत्रिक कार्य के 1kJ में परिवर्तित किया जाता है। मोटर की दक्षता क्या है? इंजन के प्रत्येक चक्र के लिए कितनी गर्मी जारी की जाती है? आकृति 13 देखें
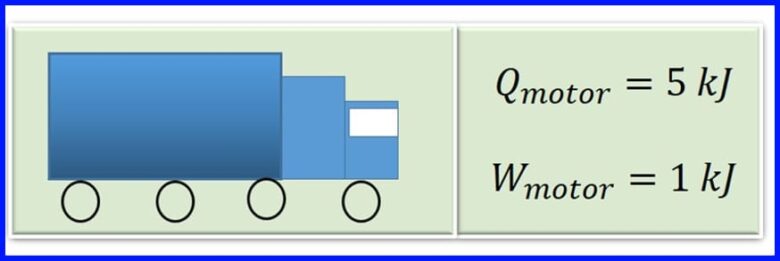
समाधान:

जारी गर्मी को निर्धारित करने के लिए, यह माना जाता है कि थर्मल मशीनों में शुद्ध कार्य प्रणाली के लिए शुद्ध गर्मी हस्तांतरण के बराबर है। आकृति 14 देखें।

Entropy:
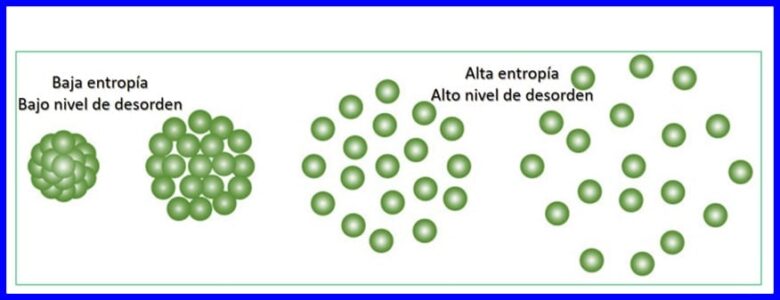
एन्ट्रॉपी एक प्रणाली में यादृच्छिकता या विकार की डिग्री है। एन्ट्रॉपी ऊर्जा के उस हिस्से को निर्धारित करना संभव बनाता है जिसका उपयोग काम का उत्पादन करने के लिए नहीं किया जा सकता है, अर्थात यह एक थर्मोडायनामिक प्रक्रिया की अपरिवर्तनीयता को निर्धारित करने की अनुमति देता है।
प्रत्येक ऊर्जा हस्तांतरण जो ब्रह्मांड के एन्ट्रापी को बढ़ाता है और काम करने के लिए उपलब्ध उपयोगी ऊर्जा की मात्रा को कम करता है। कोई भी थर्मोडायनामिक प्रक्रिया एक दिशा में आगे बढ़ेगी जो ब्रह्मांड की कुल एंट्रोपी को बढ़ाती है। आकृति 15 देखें।
3 थर्मोडायनामिक्स का नियम
थर्मोडायनामिक्स या नेरस्ट पोस्टुलेट का तीसरा नियम
ऊष्मप्रवैगिकी का तीसरा नियम तापमान और शीतलन से संबंधित है। यह बताता है कि निरपेक्ष शून्य पर एक प्रणाली का एन्ट्रापी एक निश्चित स्थिरांक है। आंकड़ा 16 देखें।
निरपेक्ष शून्य सबसे कम तापमान है जिसके नीचे अब कम माप नहीं है, यह सबसे ठंडा है जो एक शरीर हो सकता है। पूर्ण शून्य 0 K, -273,15 ºC के बराबर है।

निष्कर्ष
चार थर्मोडायनामिक सिद्धांत हैं। शून्य सिद्धांत में यह स्थापित किया जाता है कि थर्मल संतुलन तब होता है जब दो या अधिक शरीर एक ही तापमान पर होते हैं।
ऊष्मप्रवैगिकी का पहला नियम प्रक्रियाओं के बीच ऊर्जा के संरक्षण से संबंधित है, जबकि ऊष्मप्रवैगिकी का दूसरा नियम न्यूनतम से उच्चतम एंट्रोपी की दिशा से संबंधित है, और गर्मी इंजनों की दक्षता या प्रदर्शन जो गर्मी को काम में परिवर्तित करते हैं।
थर्मोडायनामिक्स का तीसरा नियम तापमान और शीतलन से संबंधित है, यह बताता है कि निरपेक्ष शून्य पर एक प्रणाली का एन्ट्रापी एक निश्चित स्थिरांक है।