Thermodynamyske prinsipes
Om op in maklike manier de brede en komplekse wrâld fan Thermodynamika te begripen, is it oan te rieden om stap foar stap te begjinnen te begjinnen mei in oersicht fan basisbegripen, in ynlieding yn thermodynamyske prinsipes, en dan yngeand de thermodynamyske wetten te bestudearjen, hoe't se wurde wiskundich útdrukt. en de tapassingen derfan.
Mei de fjouwer wetten fan 'e thermodynamika (nul wet, earste wet, twadde wet en tredde wet), wurdt beskreaun hoe't de oerdrachten en transformaasjes fan enerzjy tusken ferskate systemen wurkje; de basis wêze foar it begripen fan in protte fysika-gemyske ferskynsels fan 'e natuer.
Resinsje fan basisbegripen
Wy noegje jo út om it artikel te sjen THERMODYNAMICS, wat it is en har tapassingen

Jo kinne dizze ynformaasje oanfolje mei it artikel De krêft fan 'e wet fan Watt (tapassingen - oefeningen) Foar no Wy folgje ...
Foarmen fan enerzjy
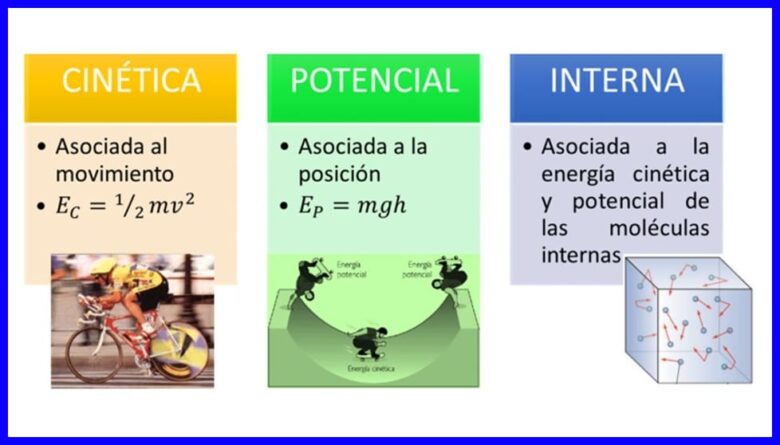
Enerzjy, it eigendom fan lichems om harsels te transformearjen troch har situaasje as steat te feroarjen, komt yn in protte foarmen, lykas kinetyske enerzjy, potensjele enerzjy en ynterne enerzjy fan lichems. Sjoch figuer 1.
Wurkje
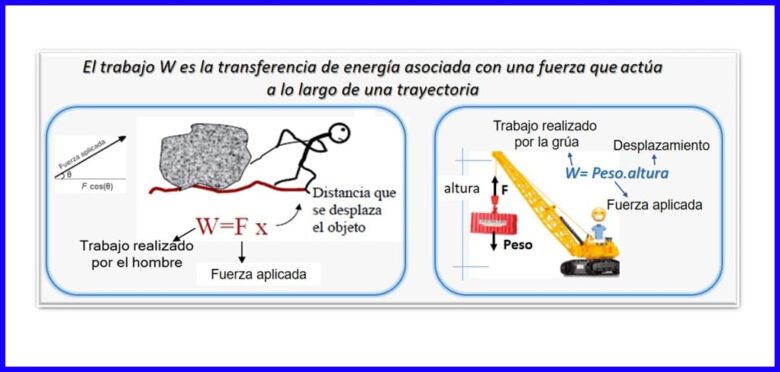
It is it produkt fan in krêft en ferpleatsing, beide mjitten yn deselde rjochting. Om it wurk te berekkenjen wurdt de komponint fan 'e krêft brûkt dy't parallel is mei de ferpleatsing fan it objekt. Wurk wurdt metten yn Nm, Joule (J), ft.lb-f, as BTU. Sjoch figuer 2.
Waarmte (Q)
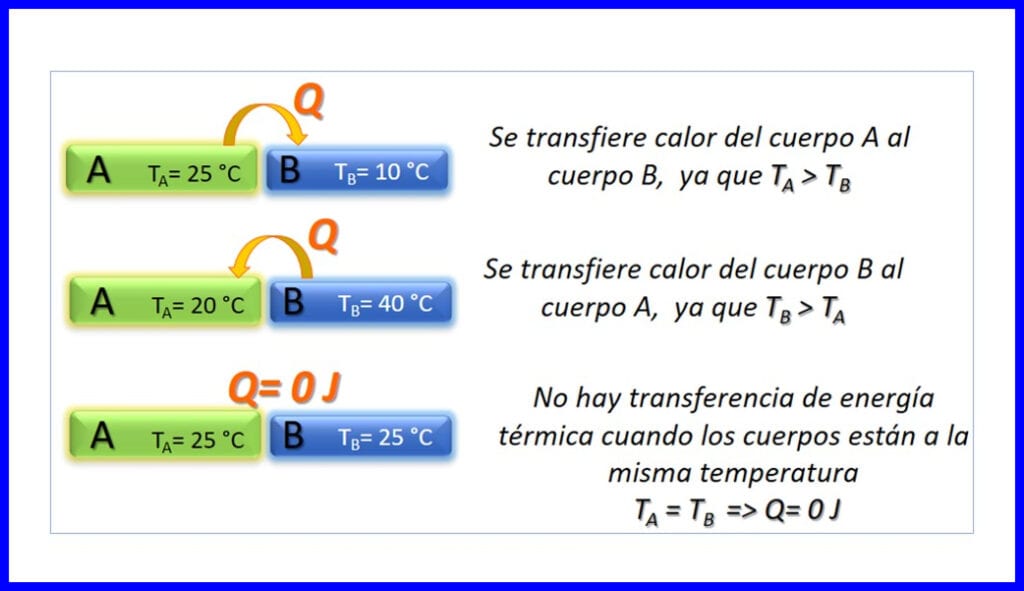
Oerdracht fan termyske enerzjy tusken twa lichems dy't op ferskillende temperatueren binne, en it komt allinich foar yn 't sin dat de temperatuer ôfnimt. Waarmte wurdt metten yn Joule, BTU, pûn-fuotten, as yn kaloryen. Sjoch figuer 3.
Thermodynamyske prinsipes
Nulrjocht - Nul prinsipe
De nulwet fan thermodynamika stelt dat as twa objekten, A en B, yn termysk lykwicht binne mei elkoar, en objekt A yn lykwicht is mei in tredde objekt C, dan is objekt B yn thermysk lykwicht mei objekt C. It thermyske lykwicht komt foar as twa of mear lichems op deselde temperatuer binne. Sjoch figuer 4.
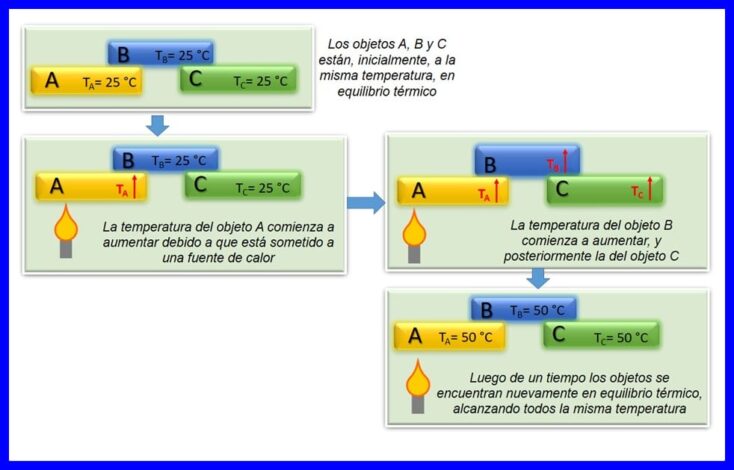
Dizze wet wurdt beskôge as in basiswet fan thermodynamika. It waard postulearre as "Zero Law", yn 1935, om't it waard postuleare nei't de earste en twadde wetten fan 'e thermodynamika waarden makke.
1ste wet fan termodynamika (prinsipe foar behâld fan enerzjy)
Ferklearring fan 'e earste wet fan termodynamika:
De earste wet fan thermodynamika, ek wol bekend as it prinsipe fan behâld fan enerzjy, stelt dat enerzjy net wurdt oanmakke of ferneatige, it wurdt allinich omfoarme ta in oar soart enerzjy, of wurdt oerbrocht fan it iene objekt nei it oare. Sadwaande feroaret de totale hoemannichte enerzjy yn it universum net.
De earste wet wurdt foltôge yn "alles", enerzjy wurdt kontinu oerdroegen en transformeare, bygelyks yn guon elektryske apparaten, lykas mixers en blenders, wurdt elektryske enerzjy omfoarme yn meganyske en thermyske enerzjy, yn it minsklik lichem wurde se de gemyske transformeare enerzjy fan iten dat yn kinetyske enerzjy wurdt opnommen as it lichem yn beweging is, of oare foarbylden lykas dy werjûn yn figuer 5.
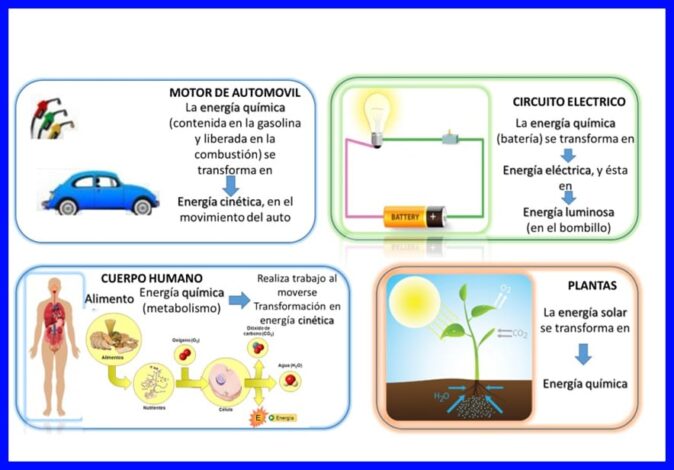
Fergeliking fan 'e earste wet fan termodynamika:
De fergeliking fan 'e earste wet binnen de thermodynamyske prinsipes ekspresje it lykwicht dat bestean moat tusken de ferskillende soarten enerzjy yn in bepaald proses. Om't, yn sletten systemen [1], de enerzjy-útwikselingen allinich kinne wurde jûn troch de oerdracht fan waarmte, of troch it dien wurk (troch of oan it systeem) wurdt fêststeld dat de enerzjyfariânsje fan in systeem gelyk is oan de som fan enerzjyferfier fia waarmte en troch wurk. Sjoch figuer 6.
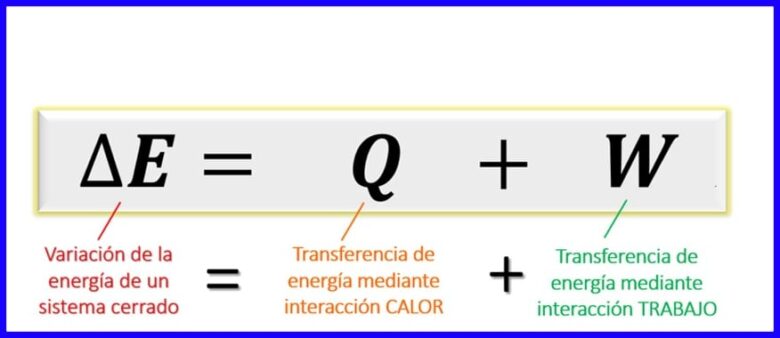
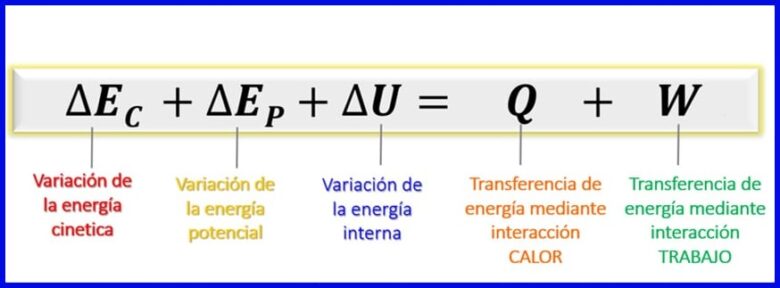
Yn betinken nommen dat de enerzjy dy't beskôge wurde yn dizze enerzjybalâns kinetyske enerzjy, potensjele enerzjy en ynterne enerzjy binne [1], bliuwt de enerzjybalâns foar sletten systemen lykas werjûn yn figuer 7.
- (ec) Kinetyske enerzjy , troch de beweging fan in lichem;
- (ep) Potensjele enerzjy, fanwegen de posysje fan in lichem yn in swiertekrêftfjild;
- (OF) Ynterne enerzjy, fanwege de mikroskopyske bydragen fan 'e kinetyske en potinsjele enerzjy fan' e ynterne molekulen fan in lichem.
Oefening 1.
In fersegele kontener befettet in stof, mei in earste enerzjy fan 10 kJ. De stof wurdt geroerd mei in propeller dy't 500 J wurket, wylst in waarmteboarne 20 kJ waarmte oerdraacht oan 'e stof. Derneist wurdt 3kJ waarmte yn 'e loft frijlitten tidens it proses. Bepale de definitive enerzjy fan 'e stof. Sjoch figuer 8.
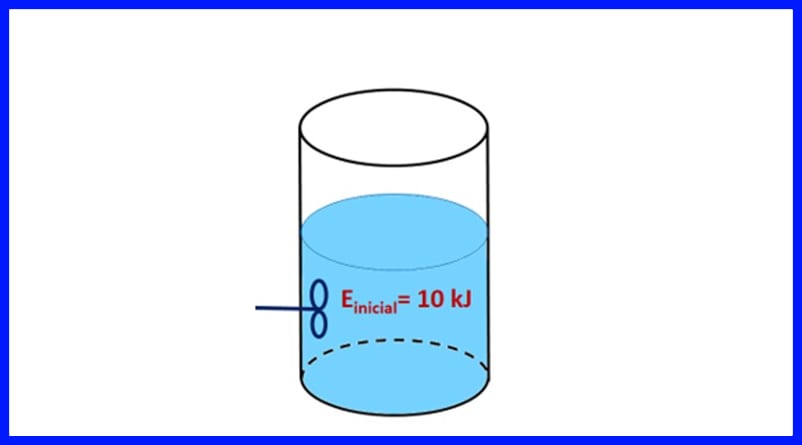
Solution:
Yn figuer 9 kinne jo de waarmte sjen tafoege troch de waarmteboarne, dy't wurdt beskôge as "posityf", om't it de enerzjy fan 'e stof fergruttet, de waarmte dy't yn' e loft frijkomt, negatyf om't it de enerzjy fan 'e substansje fermindert, wurk fan 'e propeller, dy't de enerzjy fergrutte naam in posityf teken.
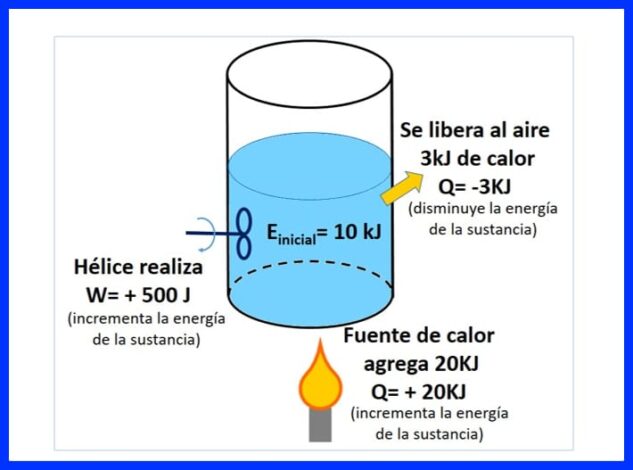
Yn figuer 10 wurdt de enerzjybalâns presinteare, neffens de earste wet fan thermodynamika en wurdt de definitive enerzjy fan 'e substansje krigen.

Twadde wet fan thermodynamika
D'r binne ferskate ferklearrings fan 'e twadde wet fan thermodynamika: Ferklearring fan Planck-Kelvin, Clausius, Carnot. Elk fan har toant in oar aspekt fan 'e twadde wet. Yn 't algemien postuleart de twadde wet fan thermodynamika:
- De rjochting fan thermodynamyske prosessen, irreversibiliteit fan fysike ferskynsels.
- De effisjinsje fan termyske masines.
- Fier it pân "entropy" yn.
Rjochting fan thermodynamyske prosessen:
Spontaan yn 'e natuer streamt of wurdt enerzjy streamd fan' e heegste enerzjysteat nei de leechste enerzjysteat. Waarmte streamt fan waarme lichems nei kâlde lichems en net oarsom. Sjoch figuer 11.

Effektiviteit as termyske prestaasjes:
Neffens de earste wet fan thermodynamika wurdt enerzjy net oanmakke noch ferneatige, mar kin it wurde transformeare of oerbrocht. Mar yn alle enerzjyferfieringen of transformaasjes is in bedrach dêrfan net nuttich om wurk te dwaan. As enerzjy wurdt oerdroegen of transformeare, wurdt in diel fan 'e earste enerzjy frijjûn as thermyske enerzjy: enerzjy degradeart, ferliest kwaliteit.
By elke enerzjytransformaasje is de verkregen enerzjy altyd minder dan de levere enerzjy. Termyske effisjinsje is de hoemannichte waarmte fan 'e boarne dy't wurdt omset yn wurk, de ferhâlding tusken de verkregen nuttige enerzjy en de enerzjy levere yn in transformaasje. Sjoch figuer 12.

Thermyske masine as hjittemasine:
De termyske masjine is in apparaat dat waarmte diels omset yn wurk as meganyske enerzjy, hjirfoar is it in boarne nedich dy't waarmte leveret op hege temperatuer.
Yn termyske masines wurdt in stof lykas wetterdamp, loft as brânstof brûkt. De stof ûndergiet in searje fan termodynamyske transformaasjes op in siklyske manier, sadat de masine kontinu kin wurkje.
Oefening 2.
De motor fan in frachtwein produseart waarmte yn ferbaarning troch benzine te ferbaarnen. Foar elke syklus fan 'e motor wurdt de waarmte fan 5 kJ omset yn 1kJ fan meganysk wurk. Wat is de effisjinsje fan 'e motor? Hoefolle waarmte wurdt frijjûn foar elke syklus fan 'e motor? Sjoch figuer 13
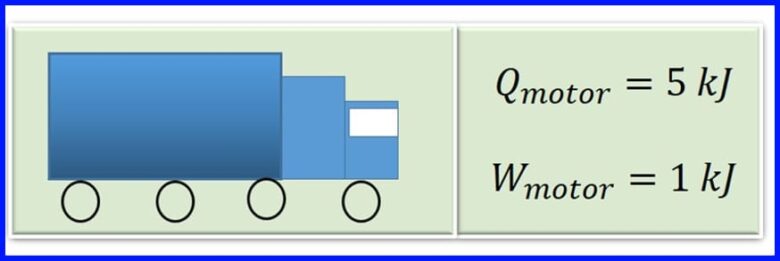
Solution:

Om de frijlizzende waarmte te bepalen, wurdt oannaam dat yn thermyske masines it netto wurk gelyk is oan 'e netto waarmteferfier nei it systeem. Sjoch figuer 14.

Entropy:
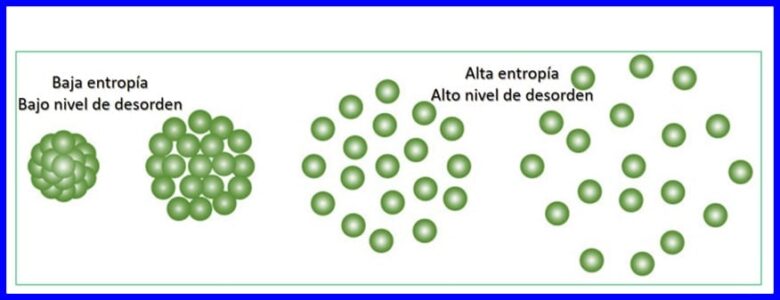
Entropy is de graad fan willekeurigens as steuring yn in systeem. Entropy lit it diel fan enerzjy kwantifisearje dat net kin wurde brûkt om wurk te produsearjen, dat wol sizze dat it de ûnomkearberens fan in thermodynamysk proses kin kwantifisearje.
Elke enerzjyferfier dy't foarkomt fergruttet de entropy fan it universum en fermindert de hoemannichte brûkbere enerzjy dy't beskikber is om wurk te dwaan. Elk thermodynamysk proses sil trochgean yn in rjochting dy't de totale entropy fan it universum fergruttet. Sjoch figuer 15.
3e wet fan termodynamika
Tredde wet fan termodynamika as Nerst Postulate
De tredde wet fan thermodynamika is relatearre oan temperatuer en koeling. It stelt dat de entropy fan in systeem by absolute nul in definitive konstante is. Sjoch figuer 16.
Absolút nul is de leechste temperatuer wêrûnder d'r net in legere mjitte is, it is de kâldste dy't in lichem kin wêze. Absolute nul is 0 K, lykweardich oan -273,15 ºC.

konklúzje
D'r binne fjouwer thermodynamyske prinsipes. Yn it nul-prinsipe wurdt fêststeld dat thermysk lykwicht optreedt as twa of mear lichems op deselde temperatuer binne.
De earste wet fan 'e thermodynamika behannelt it behâld fan enerzjy tusken prosessen, wylst de twadde wet fan' e thermodynamika behannelt fan 'e rjochting fan' e leechste nei 'e heechste entropy, en de effisjinsje of prestaasjes fan hjittemotoren dy't waarmte omsette yn wurk.
De tredde wet fan thermodynamika is relatearre oan temperatuer en koeling, it stelt dat de entropy fan in systeem op absolute nul in definitive konstant is.