اصول ترمودینامیکی
برای درک ، از یک راه آسان ، دنیای گسترده و پیچیده ترمودینامیک ، توصیه می شود گام به گام شروع کنید با بررسی اصطلاحات اساسی ، مقدمه ای بر اصول ترمودینامیکی ، و سپس مطالعه دقیق تر قوانین ترمودینامیکی ، چگونگی آنها و از نظر ریاضی بیان می شوند.
با چهار قانون ترمودینامیک (قانون صفر ، قانون اول ، قانون دوم و قانون سوم) ، نحوه کار انتقال و تبدیل انرژی بین سیستم های مختلف شرح داده شده است. مبنای درک بسیاری از پدیده های فیزیکوشیمیایی طبیعت است.
بررسی مفاهیم اساسی
ما شما را به دیدن مقاله دعوت می کنیم ترمودینامیک ، آنچه در آن است و کاربردهای آن

می توانید این اطلاعات را با مقاله تکمیل کنید قدرت قانون وات (برنامه ها - تمرینات) در حال حاضر ما دنبال می کنیم ...
اشکال انرژی
انرژی ، خاصیت اجسام برای تغییر شکل خود با تغییر وضعیت یا حالت آنها ، اشکال مختلفی دارد ، مانند انرژی جنبشی ، انرژی پتانسیل و انرژی درونی بدن. شکل 1 را ببینید.
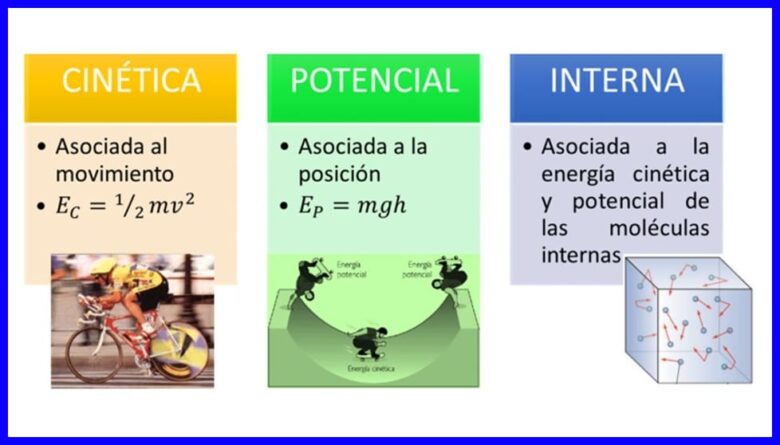
کار
این محصول یک نیرو و جابجایی است ، هر دو در یک جهت اندازه گیری می شوند. برای محاسبه کار ، از م componentلفه نیرویی که موازی با جابجایی جسم است استفاده می شود. کار با Nm ، Joule (J) ، ft.lb-f یا BTU اندازه گیری می شود. شکل 2 را ببینید.
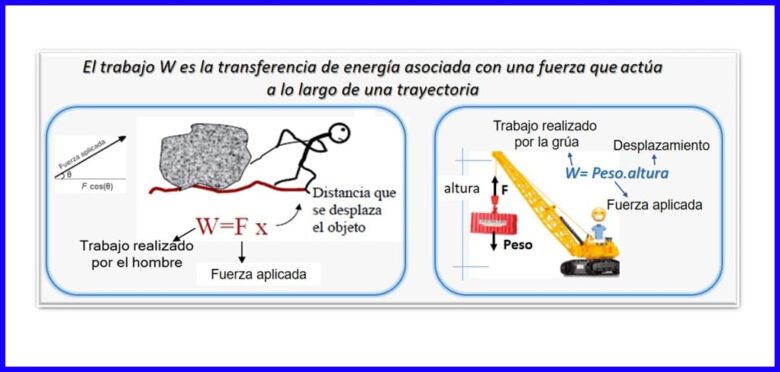
گرما (Q)
انتقال انرژی گرمایی بین دو جسمی که در دماهای مختلف هستند و فقط به این معناست که دما کاهش می یابد. گرما با ژول ، BTU ، پوند فوت یا کالری اندازه گیری می شود. شکل 3 را ببینید.
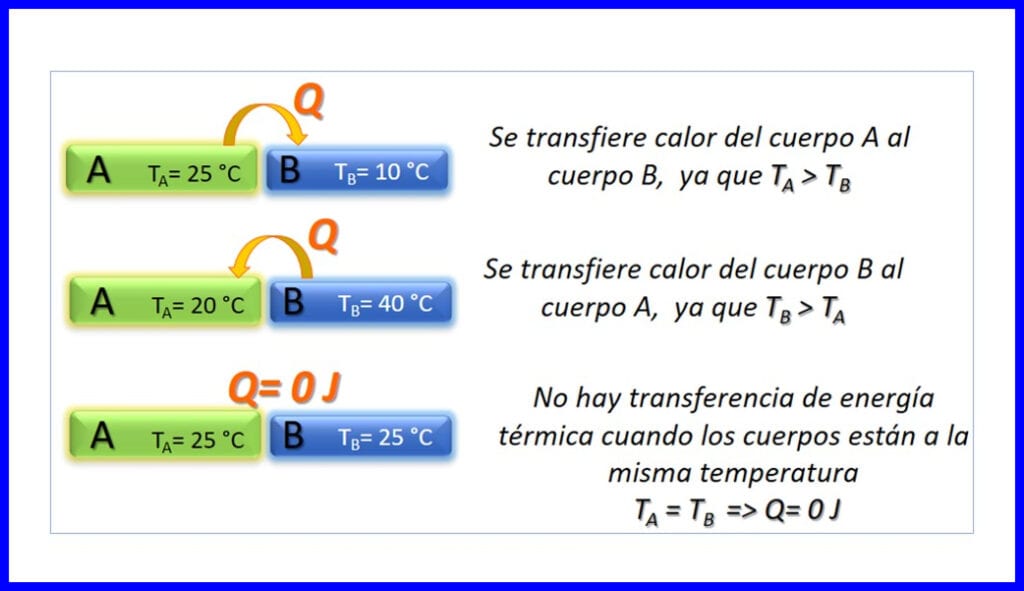
اصول ترمودینامیکی
قانون صفر - اصل صفر
قانون صفر ترمودینامیک می گوید اگر دو جسم A و B در تعادل گرمایی با یکدیگر باشند و جسم A با جسم سوم C در تعادل باشد ، پس جسم B در تعادل گرمایی با جسم C است تعادل گرمایی رخ می دهد وقتی دو یا چند جسم در یک دما هستند. شکل 4 را ببینید.
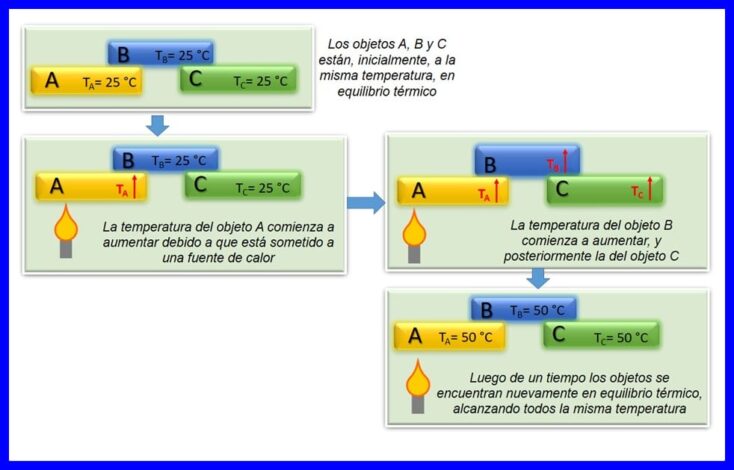
این قانون یک قانون اساسی ترمودینامیک در نظر گرفته شده است. این قانون در سال 1935 به عنوان "قانون صفر" مطرح شد ، زیرا پس از وضع قانون اول و دوم ترمودینامیک فرض شد.
قانون اول ترمودینامیک (اصل صرفه جویی در انرژی)
بیانیه قانون اول ترمودینامیک:
اولین قانون ترمودینامیک ، که به عنوان اصل صرفه جویی در انرژی نیز شناخته می شود ، بیان می کند که انرژی ایجاد یا از بین نمی رود ، فقط به نوع دیگری از انرژی تبدیل می شود یا از جسمی به جسم دیگر منتقل می شود. بنابراین مقدار کل انرژی در جهان تغییر نمی کند.
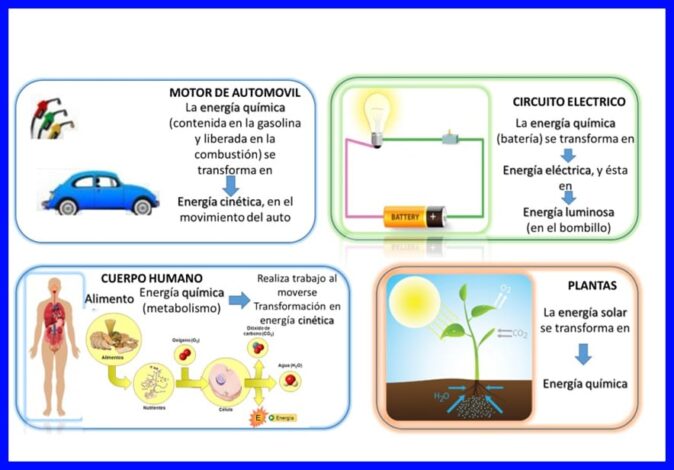
قانون اول در "همه چیز" انجام می شود ، انرژی به طور مداوم منتقل و تبدیل می شود ، به عنوان مثال ، در برخی از دستگاه های الکتریکی ، مانند میکسر و مخلوط کن ، انرژی الکتریکی به انرژی مکانیکی و حرارتی تبدیل می شود ، در بدن انسان آنها تبدیل به مواد شیمیایی می شوند انرژی غذایی که هنگام حرکت بدن به انرژی جنبشی وارد می شود یا مثالهای دیگری مانند آنچه در شکل 5 نشان داده شده است.
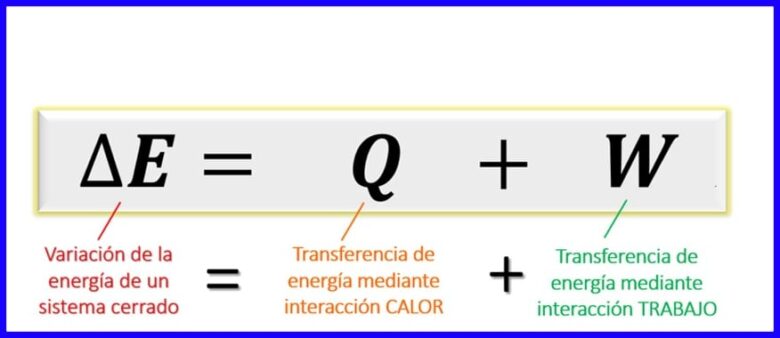
معادله قانون اول ترمودینامیک:
معادله قانون اول در اصول ترمودینامیکی تعادل را بیان می کند که باید بین انواع مختلف انرژی در یک فرآیند معین وجود داشته باشد. از آنجا که در سیستمهای بسته [1] ، مبادلات انرژی فقط با انتقال گرما یا با کار انجام شده (توسط سیستم یا بر روی سیستم) امکان پذیر است ، ثابت می شود که تغییر انرژی یک سیستم برابر است با مجموع انتقال انرژی از طریق گرما و از طریق کار. شکل 6 را ببینید.
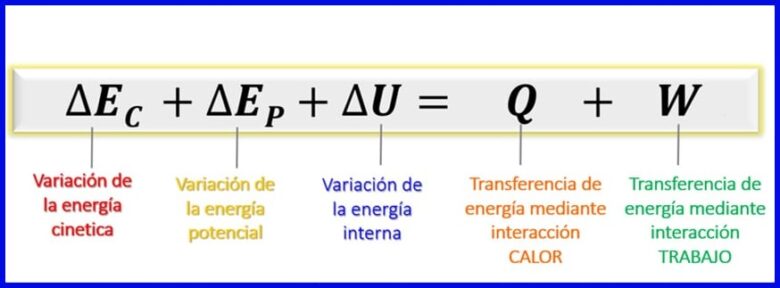
با توجه به اینکه انرژی های در نظر گرفته شده در این تعادل انرژی ، انرژی جنبشی ، انرژی پتانسیل و انرژی درونی است [1] ، تراز انرژی سیستم های بسته همچنان که در شکل 7 نشان داده شده است ، باقی می ماند.
- (ec) انرژی جنبشی ، به دلیل حرکت بدن
- (اپ) انرژی پتانسیل، به دلیل موقعیت یک بدن در یک میدان گرانشی ؛
- (یا) انرژی درونی ، به دلیل سهم میکروسکوپی انرژی جنبشی و پتانسیل مولکولهای داخلی بدن.
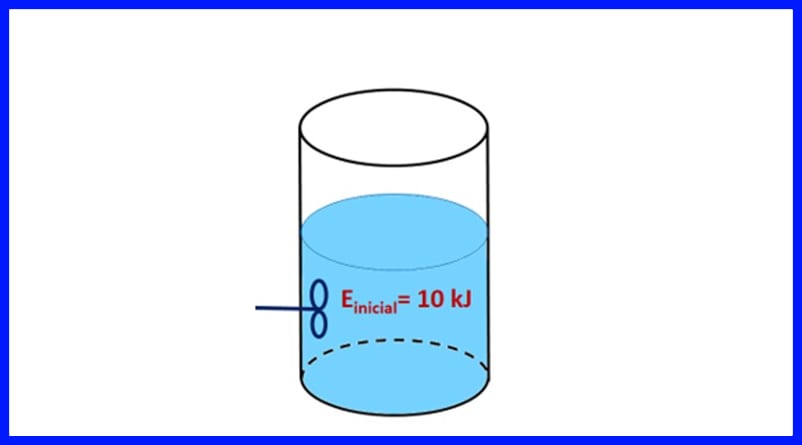
تمرین 1.
یک ظرف مهر و موم شده حاوی ماده ای با انرژی اولیه 10 کیلوژول است. این ماده با پروانه ای که 500 J کار می کند هم زده می شود ، در حالی که منبع گرما 20 کیلوژول گرما را به ماده منتقل می کند. علاوه بر این ، 3kJ گرما در طی فرآیند در هوا آزاد می شود. انرژی نهایی ماده را تعیین کنید. شکل 8 را ببینید.
راه حل:
در شکل 9 می توانید گرمای اضافه شده توسط منبع گرما را مشاهده کنید ، زیرا "مثبت" در نظر گرفته می شود زیرا باعث افزایش انرژی ماده ، گرمای آزاد شده در هوا ، منفی می شود ، زیرا انرژی ماده را کاهش می دهد و کار پروانه ، که باعث افزایش انرژی می شود ، نشانه مثبتی دارد.
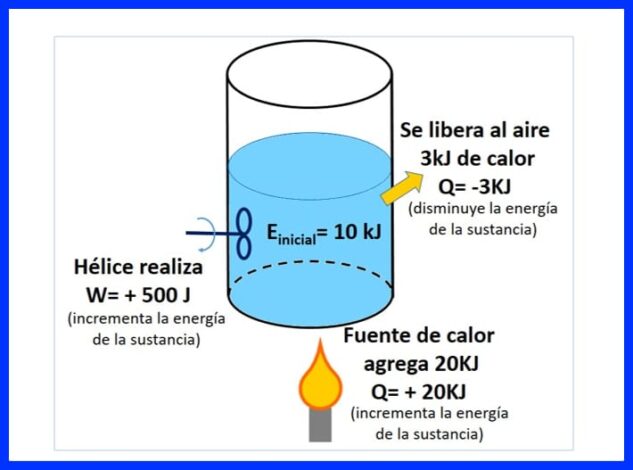
در شکل 10 تعادل انرژی ارائه شده است ، مطابق با قانون اول ترمودینامیک و انرژی نهایی ماده به دست می آید.

قانون دوم ترمودینامیک
چندین اظهارات قانون دوم ترمودینامیک وجود دارد: بیانیه پلانک-کلوین ، کلاوزیوس ، کارنو. هر یک از آنها جنبه متفاوتی از قانون دوم را نشان می دهد. به طور کلی قانون دوم ترمودینامیک فرض می کند:
- جهت فرآیندهای ترمودینامیکی ، برگشت ناپذیر پدیده های فیزیکی.
- کارایی ماشین های حرارتی.
- ویژگی "آنتروپی" را وارد کنید.
جهت فرآیندهای ترمودینامیکی:
در طبیعت خود به خود ، انرژی از بالاترین حالت انرژی به کمترین حالت انرژی جریان می یابد یا منتقل می شود. گرما از بدن داغ به بدن سرد و نه برعکس جریان می یابد. شکل 11 را ببینید.

کارایی یا عملکرد حرارتی:
طبق قانون اول ترمودینامیک ، انرژی نه ایجاد می شود و نه از بین می رود ، بلکه می تواند تبدیل یا انتقال یابد. اما در تمام انتقال یا تبدیل انرژی ، مقداری از آن برای انجام کار مفید نیست. با انتقال یا تبدیل انرژی ، بخشی از انرژی اولیه به صورت انرژی حرارتی آزاد می شود: انرژی تخریب می شود ، کیفیت را از دست می دهد.
در هر تحول انرژی ، مقدار انرژی به دست آمده همیشه کمتر از انرژی تأمین شده است. بازده حرارتی مقدار گرمای منبعی است که به کار تبدیل می شود ، نسبت بین انرژی مفید به دست آمده و انرژی تأمین شده در یک تحول. شکل 12 را ببینید.

دستگاه حرارتی یا ماشین گرمایی:
ماشین حرارتی وسیله ای است که گرما را تا حدی به انرژی کار یا مکانیکی تبدیل می کند ، برای این کار به منبعی نیاز دارد که در دمای بالا گرما تأمین کند.
در ماشین های حرارتی از ماده ای مانند بخار آب ، هوا یا سوخت استفاده می شود. این ماده به صورت چرخه ای تحت یکسری تحولات ترمودینامیکی قرار می گیرد ، به طوری که دستگاه می تواند به طور مداوم کار کند.
تمرین 2.
موتور یک وسیله نقلیه باری با سوزاندن بنزین ، گرما را در احتراق تولید می کند. برای هر چرخه موتور ، گرمای 5 کیلوژول به 1 کیلو ژول کار مکانیکی تبدیل می شود. راندمان موتور چقدر است؟ برای هر سیکل موتور چه مقدار گرما آزاد می شود؟ شکل 13 را ببینید
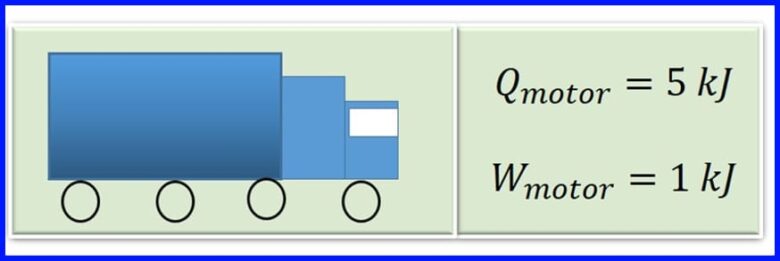
راه حل:

برای تعیین گرمای آزاد شده فرض بر این است که در ماشین های حرارتی کار خالص برابر با انتقال حرارت خالص به سیستم است. شکل 14 را ببینید.

آنتروپی:
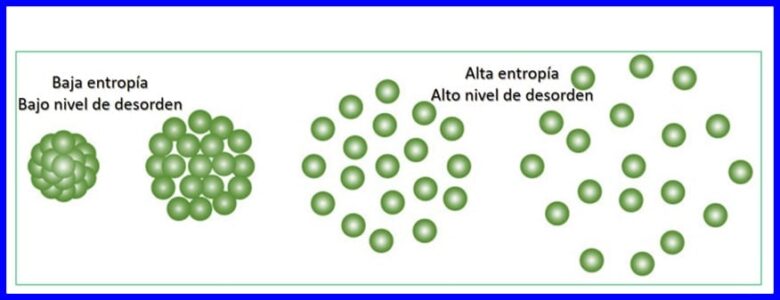
آنتروپی درجه تصادفی یا بی نظمی در یک سیستم است. آنتروپی امکان تعیین کمیت بخشی از انرژی را که نمی تواند برای تولید کار استفاده شود فراهم می کند ، یعنی امکان تعیین کمیت برگشت ناپذیری یک فرآیند ترمودینامیکی را فراهم می کند.
هر انتقال انرژی که رخ می دهد ، آنتروپی جهان را افزایش می دهد و میزان انرژی قابل استفاده برای انجام کار را کاهش می دهد. هر فرآیند ترمودینامیکی در جهتی پیش می رود که آنتروپی کل جهان را افزایش می دهد. شکل 15 را ببینید.
قانون سوم ترمودینامیک
قانون سوم ترمودینامیک یا گزاره Nerst
قانون سوم ترمودینامیک مربوط به دما و خنک سازی است. بیان می کند که آنتروپی یک سیستم در صفر مطلق یک ثابت مشخص است. شکل 16 را ببینید.
صفر مطلق کمترین دمایی است که در زیر آن دیگر اندازه گیری کمتری وجود ندارد ، این کمترین دمای بدن است. صفر مطلق 0 K ، معادل 273,15/XNUMX - .C است.

نتیجه
چهار اصل ترمودینامیکی وجود دارد. در اصل صفر مشخص شده است که تعادل گرمایی زمانی اتفاق می افتد که دو یا چند جسم در یک دما باشند.
قانون اول ترمودینامیک مربوط به صرفه جویی در انرژی بین فرآیندها است ، در حالی که قانون دوم ترمودینامیک مربوط به جهت پذیری از پایین ترین تا بالاترین آنتروپی و کارایی یا عملکرد موتورهای گرمائی است که گرما را به کار تبدیل می کنند.
قانون سوم ترمودینامیک مربوط به دما و خنک سازی است ، بیان می کند که آنتروپی یک سیستم در صفر مطلق یک ثابت مشخص است.