ਥਰਮੋਡਾਇਨਾਮਿਕ ਸਿਧਾਂਤ
ਇਹ ਸਮਝਣ ਲਈ, ਇਕ ਅਸਾਨ ਤਰੀਕੇ ਨਾਲ, ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦੀ ਵਿਸ਼ਾਲ ਅਤੇ ਗੁੰਝਲਦਾਰ ਦੁਨੀਆਂ ਨੂੰ, ਬੁਨਿਆਦੀ ਸ਼ਬਦਾਂ ਦੀ ਸਮੀਖਿਆ, ਥਰਮੋਡਾਇਨਾਮਿਕ ਸਿਧਾਂਤਾਂ ਦੀ ਜਾਣ-ਪਛਾਣ, ਅਤੇ ਫਿਰ ਵਧੇਰੇ ਡੂੰਘਾਈ ਨਾਲ ਥਰਮੋਡਾਇਨਾਮਿਕ ਕਾਨੂੰਨਾਂ ਦਾ ਅਧਿਐਨ ਕਰਦਿਆਂ, ਕਦਮ-ਕਦਮ ਜਾਣ ਦੀ ਸਿਫਾਰਸ਼ ਕੀਤੀ ਜਾਂਦੀ ਹੈ, ਉਹ ਕਿਵੇਂ. ਗਣਿਤ ਨਾਲ ਪ੍ਰਗਟ ਹੁੰਦੇ ਹਨ.
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦੇ ਚਾਰ ਕਾਨੂੰਨਾਂ (ਜ਼ੀਰੋ ਲਾਅ, ਪਹਿਲਾ ਕਾਨੂੰਨ, ਦੂਜਾ ਕਾਨੂੰਨ ਅਤੇ ਤੀਜਾ ਕਾਨੂੰਨ) ਦੇ ਨਾਲ, ਇਹ ਦੱਸਿਆ ਗਿਆ ਹੈ ਕਿ ਵੱਖ-ਵੱਖ ਪ੍ਰਣਾਲੀਆਂ ਵਿਚਕਾਰ betweenਰਜਾ ਦੀ ਤਬਦੀਲੀ ਅਤੇ ਤਬਦੀਲੀ ਕਿਵੇਂ ਕੰਮ ਕਰਦੀ ਹੈ; ਕੁਦਰਤ ਦੇ ਭੌਤਿਕ ਰਸਾਇਣਕ ਵਰਤਾਰੇ ਨੂੰ ਸਮਝਣ ਦਾ ਅਧਾਰ ਹੋਣਾ.
ਮੁ basicਲੇ ਸੰਕਲਪਾਂ ਦੀ ਸਮੀਖਿਆ
ਅਸੀਂ ਤੁਹਾਨੂੰ ਲੇਖ ਦੇਖਣ ਲਈ ਸੱਦਾ ਦਿੰਦੇ ਹਾਂ ਥਰਮੋਡਾਇਨਾਮਿਕਸ, ਇਹ ਕੀ ਹੈ ਅਤੇ ਇਸ ਦੀਆਂ ਐਪਲੀਕੇਸ਼ਨਾਂ

ਤੁਸੀਂ ਲੇਖ ਦੇ ਨਾਲ ਇਸ ਜਾਣਕਾਰੀ ਨੂੰ ਪੂਰਕ ਕਰ ਸਕਦੇ ਹੋ ਵਾਟ ਦਾ ਕਾਨੂੰਨ ਦੀ ਪਾਵਰ (ਕਾਰਜ - ਅਭਿਆਸ) ਹੁਣ ਲਈ ਅਸੀਂ ਫਾਲੋ ...
Energyਰਜਾ ਦੇ ਫਾਰਮ
Energyਰਜਾ, ਸਰੀਰ ਦੀ ਸੰਪਤੀ ਆਪਣੀ ਸਥਿਤੀ ਜਾਂ ਸਥਿਤੀ ਨੂੰ ਬਦਲ ਕੇ ਆਪਣੇ ਆਪ ਨੂੰ ਬਦਲਣ ਲਈ, ਕਈ ਰੂਪਾਂ ਵਿਚ ਆਉਂਦੀ ਹੈ, ਜਿਵੇਂ ਕਿ ਗਤੀਆਤਮਕ ,ਰਜਾ, ਸੰਭਾਵੀ energyਰਜਾ ਅਤੇ ਸਰੀਰ ਦੀ ਅੰਦਰੂਨੀ energyਰਜਾ. ਚਿੱਤਰ 1 ਵੇਖੋ.
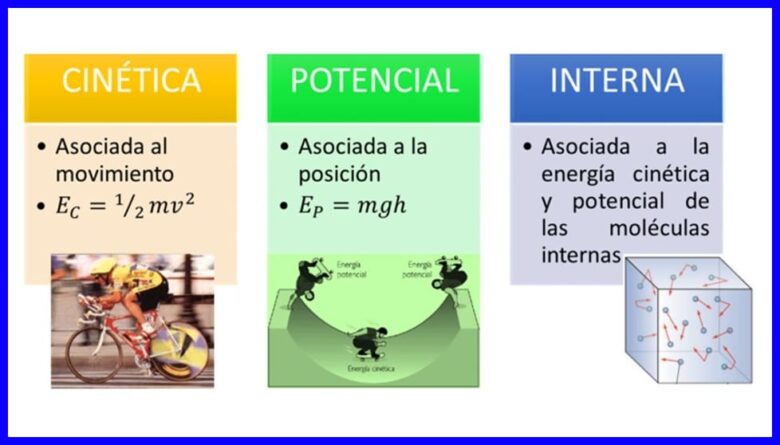
ਕੰਮ
ਇਹ ਇਕ ਸ਼ਕਤੀ ਅਤੇ ਵਿਸਥਾਪਨ ਦਾ ਉਤਪਾਦ ਹੈ, ਦੋਵੇਂ ਇਕੋ ਦਿਸ਼ਾ ਵਿਚ ਮਾਪੇ ਜਾਂਦੇ ਹਨ. ਕੰਮ ਦੀ ਗਣਨਾ ਕਰਨ ਲਈ, ਤਾਕਤ ਦਾ ਉਹ ਭਾਗ ਜੋ ਆਬਜੈਕਟ ਦੇ ਵਿਸਥਾਪਨ ਦੇ ਸਮਾਨ ਹੈ ਵਰਤੇ ਜਾਂਦੇ ਹਨ. ਕੰਮ ਨੂੰ ਐਨ ਐਮ, ਜੌਲੇ (ਜੇ), ft.lb-f, ਜਾਂ BTU ਵਿੱਚ ਮਾਪਿਆ ਜਾਂਦਾ ਹੈ. ਚਿੱਤਰ 2 ਵੇਖੋ.
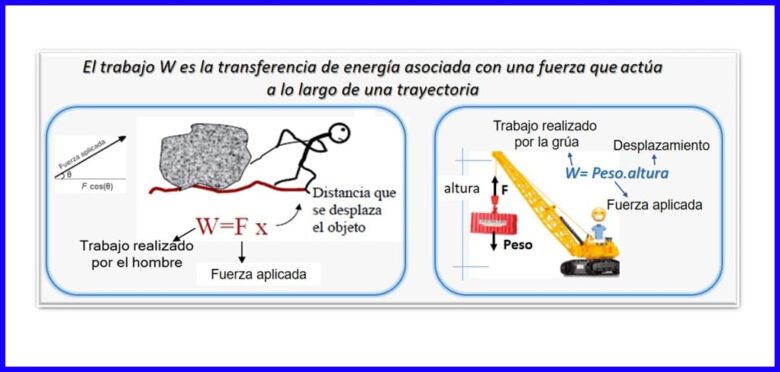
ਗਰਮੀ (ਕਿ))
ਥਰਮਲ temperaturesਰਜਾ ਦਾ ਦੋ ਸੰਸਥਾਵਾਂ ਵਿਚ ਤਬਦੀਲ ਹੋਣਾ ਜੋ ਵੱਖੋ ਵੱਖਰੇ ਤਾਪਮਾਨਾਂ ਤੇ ਹੁੰਦੇ ਹਨ, ਅਤੇ ਇਹ ਸਿਰਫ ਇਸ ਅਰਥ ਵਿਚ ਹੁੰਦਾ ਹੈ ਕਿ ਤਾਪਮਾਨ ਘਟਦਾ ਹੈ. ਗਰਮੀ ਨੂੰ ਜੌਲੇ, ਬੀਟੀਯੂ, ਪੌਂਡ-ਫੁੱਟ ਜਾਂ ਕੈਲੋਰੀ ਵਿਚ ਮਾਪਿਆ ਜਾਂਦਾ ਹੈ. ਚਿੱਤਰ 3 ਵੇਖੋ.
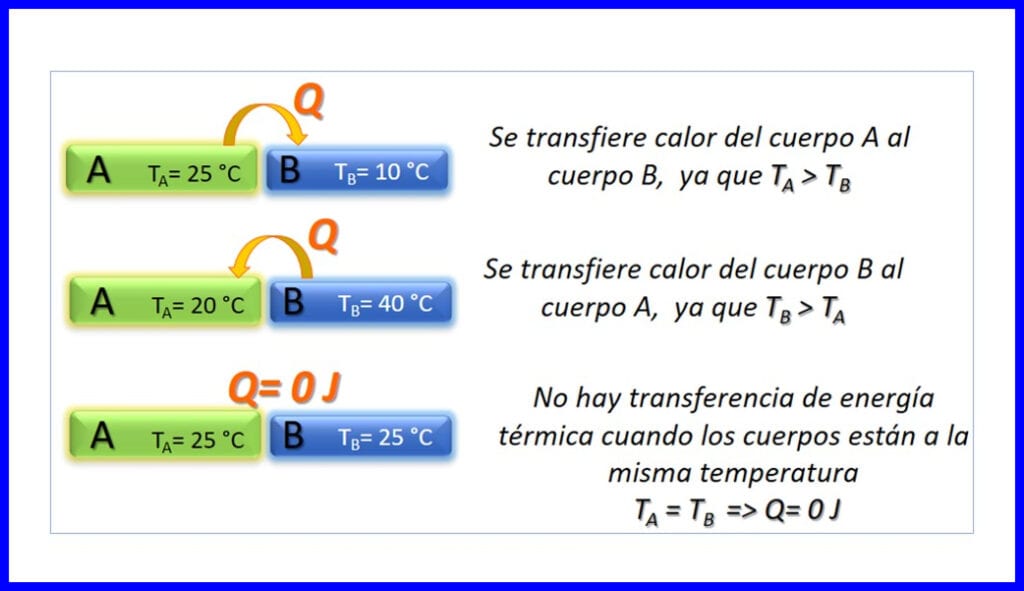
ਥਰਮੋਡਾਇਨਾਮਿਕ ਸਿਧਾਂਤ
ਜ਼ੀਰੋ ਲਾਅ - ਜ਼ੀਰੋ ਸਿਧਾਂਤ
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਜ਼ੀਰੋ ਨਿਯਮ ਕਹਿੰਦਾ ਹੈ ਕਿ ਜੇ ਦੋ ਆਬਜੈਕਟ, ਏ ਅਤੇ ਬੀ ਇਕ ਦੂਜੇ ਦੇ ਨਾਲ ਥਰਮਲ ਸੰਤੁਲਨ ਵਿਚ ਹਨ, ਅਤੇ ਇਕਾਈ ਤੀਜੀ ਇਕਾਈ ਸੀ ਦੇ ਨਾਲ ਸੰਤੁਲਨ ਵਿਚ ਹੈ, ਤਾਂ ਆਬਜੈਕਟ ਬੀ ਇਕਾਈ ਦੇ ਨਾਲ ਥਰਮਲ ਸੰਤੁਲਨ ਵਿਚ ਹੁੰਦਾ ਹੈ. ਥਰਮਲ ਸੰਤੁਲਨ ਹੁੰਦਾ ਹੈ. ਜਦੋਂ ਦੋ ਜਾਂ ਵਧੇਰੇ ਲਾਸ਼ ਇੱਕੋ ਤਾਪਮਾਨ ਤੇ ਹੁੰਦੇ ਹਨ. ਚਿੱਤਰ 4 ਵੇਖੋ.
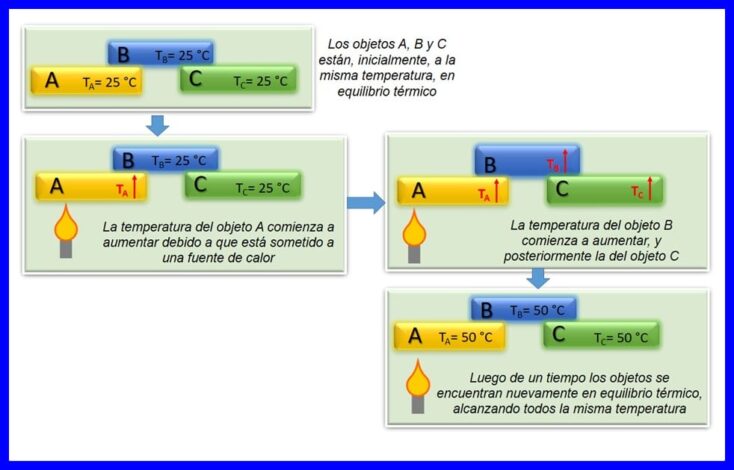
ਇਹ ਕਾਨੂੰਨ ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਮੁ basicਲਾ ਕਾਨੂੰਨ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ. ਇਸਨੂੰ 1935 ਵਿਚ "ਜ਼ੀਰੋ ਲਾਅ" ਕਿਹਾ ਜਾਂਦਾ ਸੀ, ਕਿਉਂਕਿ ਇਹ ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦੇ ਪਹਿਲੇ ਅਤੇ ਦੂਸਰੇ ਕਾਨੂੰਨ ਬਣਨ ਤੋਂ ਬਾਅਦ ਤਿਆਰ ਕੀਤਾ ਗਿਆ ਸੀ.
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਪਹਿਲਾ ਕਾਨੂੰਨ (ofਰਜਾ ਦੀ ਸੰਭਾਲ ਦਾ ਸਿਧਾਂਤ)
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦੇ ਪਹਿਲੇ ਕਾਨੂੰਨ ਦਾ ਬਿਆਨ:
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਪਹਿਲਾ ਕਾਨੂੰਨ, ਜਿਸ ਨੂੰ energyਰਜਾ ਦੀ ਸੰਭਾਲ ਦੇ ਸਿਧਾਂਤ ਵਜੋਂ ਵੀ ਜਾਣਿਆ ਜਾਂਦਾ ਹੈ, ਕਹਿੰਦਾ ਹੈ ਕਿ energyਰਜਾ ਪੈਦਾ ਨਹੀਂ ਹੁੰਦੀ ਜਾਂ ਨਸ਼ਟ ਨਹੀਂ ਹੁੰਦੀ, ਇਹ ਸਿਰਫ ਇਕ ਹੋਰ ਕਿਸਮ ਦੀ intoਰਜਾ ਵਿਚ ਬਦਲ ਜਾਂਦੀ ਹੈ, ਜਾਂ ਇਹ ਇਕ ਵਸਤੂ ਤੋਂ ਦੂਜੀ ਵਿਚ ਤਬਦੀਲ ਹੋ ਜਾਂਦੀ ਹੈ. ਇਸ ਤਰ੍ਹਾਂ ਬ੍ਰਹਿਮੰਡ ਵਿਚ energyਰਜਾ ਦੀ ਕੁੱਲ ਮਾਤਰਾ ਨਹੀਂ ਬਦਲਦੀ.
ਪਹਿਲਾ ਕਾਨੂੰਨ “ਹਰ ਚੀਜ਼” ਵਿਚ ਪੂਰਾ ਹੁੰਦਾ ਹੈ, energyਰਜਾ ਦਾ ਤਬਾਦਲਾ ਅਤੇ ਨਿਰੰਤਰ ਰੂਪ ਵਿਚ ਬਦਲਿਆ ਜਾਂਦਾ ਹੈ, ਉਦਾਹਰਣ ਵਜੋਂ, ਕੁਝ ਬਿਜਲੀ ਯੰਤਰਾਂ ਵਿਚ, ਜਿਵੇਂ ਕਿ ਮਿਕਸਰ ਅਤੇ ਬਲੈਡਰ, ਇਲੈਕਟ੍ਰਿਕ energyਰਜਾ ਮਕੈਨੀਕਲ ਅਤੇ ਥਰਮਲ intoਰਜਾ ਵਿਚ ਬਦਲ ਜਾਂਦੀ ਹੈ, ਮਨੁੱਖੀ ਸਰੀਰ ਵਿਚ ਉਹ ਰਸਾਇਣ ਨੂੰ ਬਦਲਦੇ ਹਨ ਭੋਜਨ ਦੀ energyਰਜਾ ਜਿਹੜੀ ਗਤੀਸ਼ੀਲ energyਰਜਾ ਵਿਚ ਪਾਈ ਜਾਂਦੀ ਹੈ ਜਦੋਂ ਸਰੀਰ ਗਤੀਸ਼ੀਲ ਹੁੰਦਾ ਹੈ, ਜਾਂ ਹੋਰ ਉਦਾਹਰਣਾਂ ਜਿਵੇਂ ਕਿ ਚਿੱਤਰ 5 ਵਿਚ ਦਰਸਾਈਆਂ ਗਈਆਂ ਹਨ.
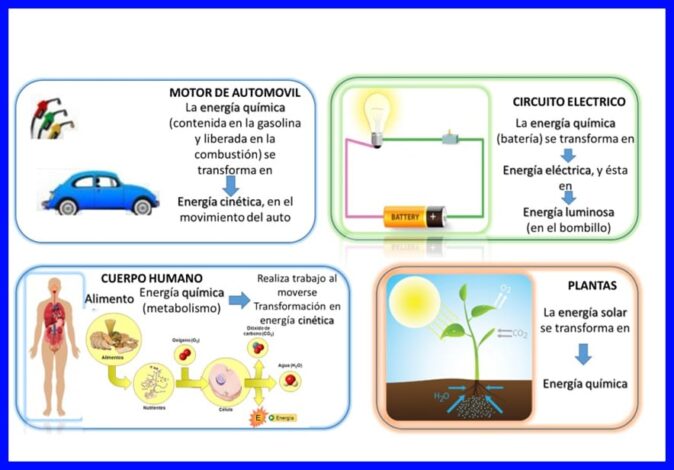
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦੇ ਪਹਿਲੇ ਕਾਨੂੰਨ ਦਾ ਸਮੀਕਰਨ:
ਥਰਮੋਡਾਇਨਾਮਿਕ ਸਿਧਾਂਤਾਂ ਦੇ ਅੰਦਰ ਪਹਿਲੇ ਕਾਨੂੰਨ ਦਾ ਸਮੀਕਰਨ ਸੰਤੁਲਨ ਨੂੰ ਜ਼ਾਹਰ ਕਰਦਾ ਹੈ ਜੋ ਕਿਸੇ ਨਿਰਧਾਰਤ ਪ੍ਰਕਿਰਿਆ ਵਿੱਚ ਵੱਖ ਵੱਖ ਕਿਸਮਾਂ ਦੀ energyਰਜਾ ਦੇ ਵਿਚਕਾਰ ਮੌਜੂਦ ਹੋਣਾ ਚਾਹੀਦਾ ਹੈ. ਕਿਉਂਕਿ, ਬੰਦ ਸਿਸਟਮ [1] ਵਿੱਚ, energyਰਜਾ ਦਾ ਆਦਾਨ-ਪ੍ਰਦਾਨ ਸਿਰਫ ਗਰਮੀ ਦੇ ਤਬਾਦਲੇ ਦੁਆਰਾ ਦਿੱਤਾ ਜਾ ਸਕਦਾ ਹੈ, ਜਾਂ ਕੀਤੇ ਕੰਮ (ਸਿਸਟਮ ਦੁਆਰਾ ਜਾਂ ਦੁਆਰਾ) ਦੁਆਰਾ, ਇਹ ਸਥਾਪਿਤ ਕੀਤਾ ਜਾਂਦਾ ਹੈ ਕਿ ਇੱਕ ਸਿਸਟਮ ਦੀ systemਰਜਾ ਪਰਿਵਰਤਨ ਦੀ ਰਕਮ ਦੇ ਬਰਾਬਰ ਹੈ ਗਰਮੀ ਅਤੇ ਕੰਮ ਦੁਆਰਾ energyਰਜਾ ਸੰਚਾਰ. ਚਿੱਤਰ 6 ਵੇਖੋ.
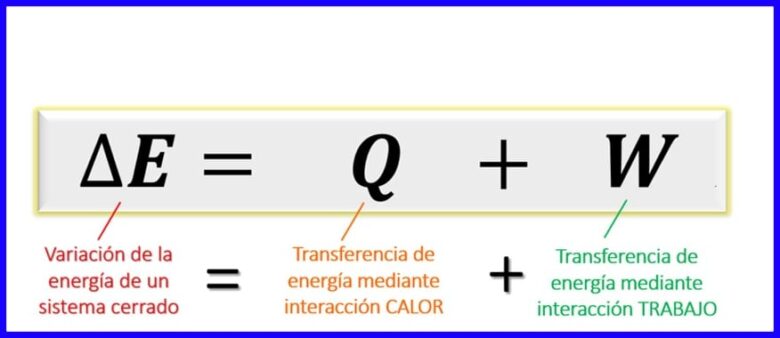
ਇਹ ਧਿਆਨ ਵਿੱਚ ਰੱਖਦੇ ਹੋਏ ਕਿ ਇਸ energyਰਜਾ ਸੰਤੁਲਨ ਵਿੱਚ ਵਿਚਾਰੀਆਂ ਗਈਆਂ consideredਰਜਾ ਗਤੀਆਤਮਕ ,ਰਜਾ, ਸੰਭਾਵੀ energyਰਜਾ ਅਤੇ ਅੰਦਰੂਨੀ energyਰਜਾ [1] ਹਨ, ਬੰਦ ਪ੍ਰਣਾਲੀਆਂ ਲਈ balanceਰਜਾ ਸੰਤੁਲਨ ਚਿੱਤਰ 7 ਵਿੱਚ ਦਰਸਾਏ ਅਨੁਸਾਰ ਹੈ.
- (ਈਸੀ) ਗਤੀਆਤਮਿਕ ਊਰਜਾ , ਕਿਸੇ ਸਰੀਰ ਦੀ ਗਤੀ ਦੇ ਕਾਰਨ;
- (ਐਪੀ) ਸੰਭਾਵੀ ਊਰਜਾ, ਇਕ ਗੁਰੂਤਾ ਖੇਤਰ ਵਿਚ ਸਰੀਰ ਦੀ ਸਥਿਤੀ ਦੇ ਕਾਰਨ;
- (ਯੂ) ਅੰਦਰੂਨੀ energyਰਜਾ, ਕਿਸੇ ਸਰੀਰ ਦੇ ਅੰਦਰੂਨੀ ਅਣੂ ਦੇ ਗਤੀਸ਼ੀਲ ਅਤੇ ਸੰਭਾਵੀ energyਰਜਾ ਦੇ ਸੂਖਮ ਯੋਗਦਾਨਾਂ ਕਾਰਨ.
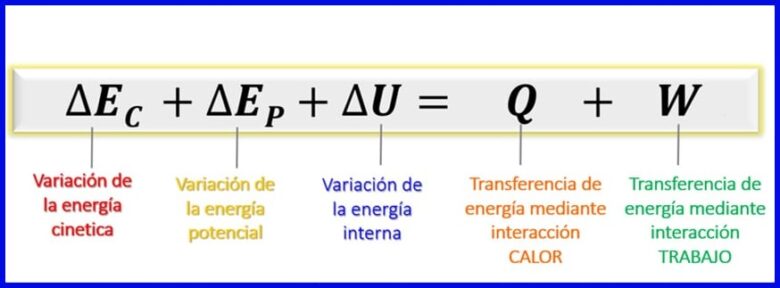
ਕਸਰਤ 1.
ਸੀਲਬੰਦ ਡੱਬੇ ਵਿਚ ਇਕ ਪਦਾਰਥ ਹੁੰਦਾ ਹੈ, ਜਿਸ ਵਿਚ ਸ਼ੁਰੂਆਤੀ energyਰਜਾ 10 ਕੇਜੇ ਹੁੰਦੀ ਹੈ. ਪਦਾਰਥ ਨੂੰ ਇੱਕ ਪ੍ਰੋਪੈਲਰ ਨਾਲ ਭੜਕਾਇਆ ਜਾਂਦਾ ਹੈ ਜੋ 500 ਜੇ ਕੰਮ ਕਰਦਾ ਹੈ, ਜਦੋਂ ਕਿ ਇੱਕ ਗਰਮੀ ਦਾ ਸਰੋਤ ਪਦਾਰਥ ਵਿੱਚ 20 ਕੇਜੇ ਗਰਮੀ ਨੂੰ ਤਬਦੀਲ ਕਰਦਾ ਹੈ. ਇਸ ਤੋਂ ਇਲਾਵਾ, ਪ੍ਰਕਿਰਿਆ ਦੇ ਦੌਰਾਨ 3kJ ਗਰਮੀ ਹਵਾ ਵਿੱਚ ਛੱਡ ਦਿੱਤੀ ਜਾਂਦੀ ਹੈ. ਪਦਾਰਥ ਦੀ ਅੰਤਮ energyਰਜਾ ਨਿਰਧਾਰਤ ਕਰੋ. ਚਿੱਤਰ 8 ਵੇਖੋ.
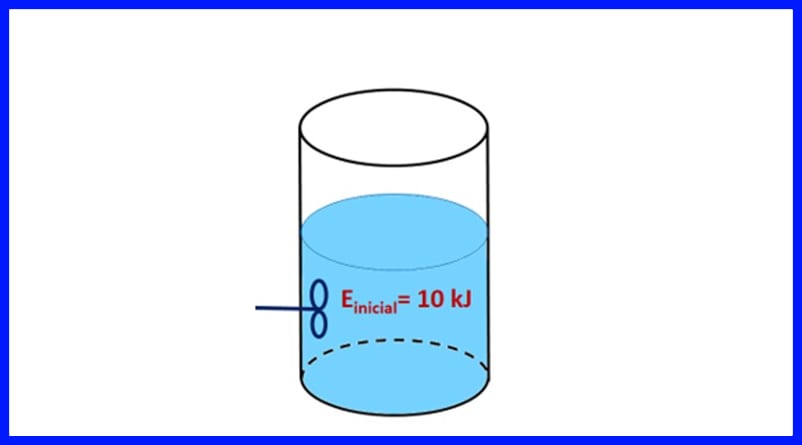
ਹੱਲ:
ਚਿੱਤਰ 9 ਵਿਚ ਤੁਸੀਂ ਗਰਮੀ ਦੇ ਸਰੋਤ ਦੁਆਰਾ ਜੋੜੀ ਗਈ ਗਰਮੀ ਨੂੰ ਦੇਖ ਸਕਦੇ ਹੋ, ਜਿਸ ਨੂੰ "ਸਕਾਰਾਤਮਕ" ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ ਕਿਉਂਕਿ ਇਹ ਪਦਾਰਥ ਦੀ increasesਰਜਾ ਨੂੰ ਵਧਾਉਂਦਾ ਹੈ, ਗਰਮੀ ਜੋ ਹਵਾ ਵਿਚ ਜਾਰੀ ਹੁੰਦੀ ਹੈ, ਨਕਾਰਾਤਮਕ ਹੈ ਕਿਉਂਕਿ ਇਹ ਪਦਾਰਥ ਦੀ decreਰਜਾ ਨੂੰ ਘਟਾਉਂਦੀ ਹੈ, ਅਤੇ ਹੇਲਿਕਸ ਦਾ ਕੰਮ, ਜਿਸ ਨਾਲ increasedਰਜਾ ਵੱਧ ਗਈ ਇਕ ਸਕਾਰਾਤਮਕ ਸੰਕੇਤ ਹੈ.
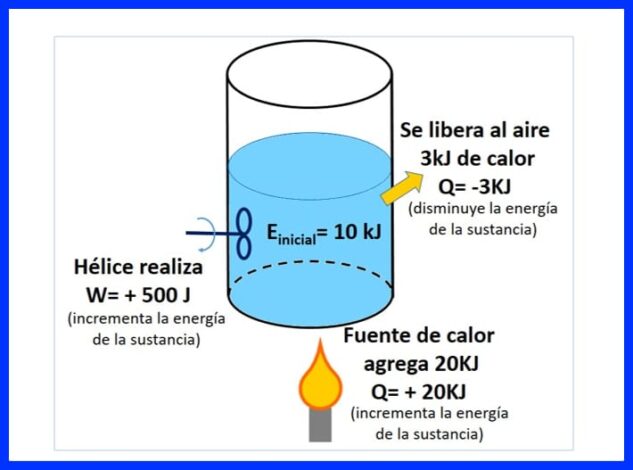
ਚਿੱਤਰ 10 ਵਿਚ mਰਜਾ ਸੰਤੁਲਨ ਪੇਸ਼ ਕੀਤਾ ਜਾਂਦਾ ਹੈ, ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦੇ ਪਹਿਲੇ ਕਾਨੂੰਨ ਅਨੁਸਾਰ ਅਤੇ ਪਦਾਰਥ ਦੀ ਅੰਤਮ energyਰਜਾ ਪ੍ਰਾਪਤ ਕੀਤੀ ਜਾਂਦੀ ਹੈ.

ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਦੂਜਾ ਕਾਨੂੰਨ
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦੇ ਦੂਸਰੇ ਕਾਨੂੰਨ ਦੇ ਕਈ ਬਿਆਨ ਹਨ: ਪਲੈਂਕ-ਕੈਲਵਿਨ, ਕਲਾਸੀਅਸ, ਕਾਰਨੋਟ ਦਾ ਬਿਆਨ. ਉਨ੍ਹਾਂ ਵਿਚੋਂ ਹਰੇਕ ਦੂਜੇ ਕਾਨੂੰਨ ਦਾ ਇਕ ਵੱਖਰਾ ਪਹਿਲੂ ਦਰਸਾਉਂਦਾ ਹੈ. ਆਮ ਤੌਰ ਤੇ ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਦੂਜਾ ਨਿਯਮ ਸੰਕੇਤ ਕਰਦਾ ਹੈ:
- ਥਰਮੋਡਾਇਨਾਮਿਕ ਪ੍ਰਕਿਰਿਆਵਾਂ ਦੀ ਦਿਸ਼ਾ, ਸਰੀਰਕ ਵਰਤਾਰੇ ਦੀ ਅਟੱਲਤਾ.
- ਥਰਮਲ ਮਸ਼ੀਨਾਂ ਦੀ ਕੁਸ਼ਲਤਾ.
- ਵਿਸ਼ੇਸ਼ਤਾ "ਐਂਟਰੋਪੀ" ਦਾਖਲ ਕਰੋ.
ਥਰਮੋਡਾਇਨਾਮਿਕ ਪ੍ਰਕਿਰਿਆਵਾਂ ਦੀ ਦਿਸ਼ਾ:
ਕੁਦਰਤ ਵਿੱਚ, energyਰਜਾ ਵਹਿੰਦੀ ਹੈ ਜਾਂ ਸਭ ਤੋਂ ਉੱਚੇ energyਰਜਾ ਰਾਜ ਤੋਂ ਹੇਠਲੇ energyਰਜਾ ਰਾਜ ਵਿੱਚ ਤਬਦੀਲ ਕੀਤੀ ਜਾਂਦੀ ਹੈ. ਗਰਮੀ ਗਰਮ ਸਰੀਰ ਤੋਂ ਠੰਡੇ ਸਰੀਰਾਂ ਵੱਲ ਵਗਦੀ ਹੈ ਨਾ ਕਿ ਦੂਜੇ ਪਾਸੇ. ਚਿੱਤਰ 11 ਵੇਖੋ.

ਕੁਸ਼ਲਤਾ ਜਾਂ ਥਰਮਲ ਪ੍ਰਦਰਸ਼ਨ:
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦੇ ਪਹਿਲੇ ਕਾਨੂੰਨ ਦੇ ਅਨੁਸਾਰ, neitherਰਜਾ ਨਾ ਤਾਂ ਬਣਾਈ ਜਾਂਦੀ ਹੈ ਅਤੇ ਨਾ ਹੀ ਨਸ਼ਟ ਹੁੰਦੀ ਹੈ, ਬਲਕਿ ਇਸਨੂੰ ਬਦਲਿਆ ਜਾਂ ਤਬਦੀਲ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ. ਪਰ ਸਾਰੀਆਂ energyਰਜਾ ਤਬਦੀਲੀਆਂ ਜਾਂ ਤਬਦੀਲੀਆਂ ਵਿੱਚ ਇਸਦਾ ਇੱਕ ਹਿੱਸਾ ਕੰਮ ਕਰਨਾ ਲਾਭਦਾਇਕ ਨਹੀਂ ਹੁੰਦਾ. ਜਿਵੇਂ ਕਿ energyਰਜਾ ਦਾ ਤਬਾਦਲਾ ਜਾਂ ਪਰਿਵਰਤਨ ਹੁੰਦਾ ਹੈ, ਸ਼ੁਰੂਆਤੀ energyਰਜਾ ਦਾ ਕੁਝ ਹਿੱਸਾ ਥਰਮਲ energyਰਜਾ ਦੇ ਤੌਰ ਤੇ ਜਾਰੀ ਕੀਤਾ ਜਾਂਦਾ ਹੈ: energyਰਜਾ ਘੱਟ ਜਾਂਦੀ ਹੈ, ਗੁਣ ਗੁਆਉਂਦੀ ਹੈ.
ਕਿਸੇ ਵੀ transਰਜਾ ਤਬਦੀਲੀ ਵਿੱਚ, ਪ੍ਰਾਪਤ ਕੀਤੀ energyਰਜਾ ਦੀ ਮਾਤਰਾ ਹਮੇਸ਼ਾਂ ਪ੍ਰਦਾਨ ਕੀਤੀ energyਰਜਾ ਨਾਲੋਂ ਘੱਟ ਹੁੰਦੀ ਹੈ. ਥਰਮਲ ਕੁਸ਼ਲਤਾ ਸਰੋਤ ਤੋਂ ਗਰਮੀ ਦੀ ਮਾਤਰਾ ਹੈ ਜੋ ਕੰਮ ਵਿੱਚ ਬਦਲ ਜਾਂਦੀ ਹੈ, ਪ੍ਰਾਪਤ ਕੀਤੀ ਉਪਯੋਗੀ energyਰਜਾ ਅਤੇ ਇੱਕ ਤਬਦੀਲੀ ਵਿੱਚ ਦਿੱਤੀ ਗਈ betweenਰਜਾ ਦੇ ਵਿਚਕਾਰ ਅਨੁਪਾਤ ਹੈ. ਚਿੱਤਰ 12 ਵੇਖੋ.

ਥਰਮਲ ਮਸ਼ੀਨ ਜਾਂ ਹੀਟ ਮਸ਼ੀਨ:
ਥਰਮਲ ਮਸ਼ੀਨ ਇੱਕ ਉਪਕਰਣ ਹੈ ਜੋ ਅੰਸ਼ਕ ਤੌਰ ਤੇ ਗਰਮੀ ਨੂੰ ਕੰਮ ਜਾਂ ਮਕੈਨੀਕਲ energyਰਜਾ ਵਿੱਚ ਬਦਲਦਾ ਹੈ, ਇਸਦੇ ਲਈ ਇਸਨੂੰ ਇੱਕ ਸਰੋਤ ਦੀ ਜਰੂਰਤ ਹੁੰਦੀ ਹੈ ਜੋ ਉੱਚ ਤਾਪਮਾਨ ਤੇ ਗਰਮੀ ਦੀ ਸਪਲਾਈ ਕਰਦਾ ਹੈ.
ਥਰਮਲ ਮਸ਼ੀਨਾਂ ਵਿਚ ਇਕ ਪਦਾਰਥ ਜਿਵੇਂ ਪਾਣੀ ਦੀ ਭਾਫ਼, ਹਵਾ ਜਾਂ ਬਾਲਣ ਦੀ ਵਰਤੋਂ ਕੀਤੀ ਜਾਂਦੀ ਹੈ. ਪਦਾਰਥ ਚੱਕਰਵਾਤੀ inੰਗ ਨਾਲ ਥਰਮੋਡਾਇਨਾਮਿਕ ਤਬਦੀਲੀਆਂ ਦੀ ਲੜੀ ਵਿਚੋਂ ਲੰਘਦਾ ਹੈ, ਤਾਂ ਜੋ ਮਸ਼ੀਨ ਨਿਰੰਤਰ ਕੰਮ ਕਰ ਸਕੇ.
ਕਸਰਤ 2.
ਕਾਰਗੋ ਵਾਹਨ ਦਾ ਇੰਜਣ ਗੈਸੋਲੀਨ ਸਾੜ ਕੇ ਬਲਨ ਵਿਚ ਗਰਮੀ ਪੈਦਾ ਕਰਦਾ ਹੈ. ਇੰਜਣ ਦੇ ਹਰੇਕ ਚੱਕਰ ਲਈ, 5 ਕੇਜੇ ਦੀ ਗਰਮੀ ਨੂੰ 1KJ ਵਿੱਚ ਮਕੈਨੀਕਲ ਕੰਮ ਵਿੱਚ ਬਦਲਿਆ ਜਾਂਦਾ ਹੈ. ਮੋਟਰ ਦੀ ਕੁਸ਼ਲਤਾ ਕੀ ਹੈ? ਇੰਜਣ ਦੇ ਹਰੇਕ ਚੱਕਰ ਲਈ ਕਿੰਨੀ ਗਰਮੀ ਜਾਰੀ ਕੀਤੀ ਜਾਂਦੀ ਹੈ? ਚਿੱਤਰ 13 ਵੇਖੋ
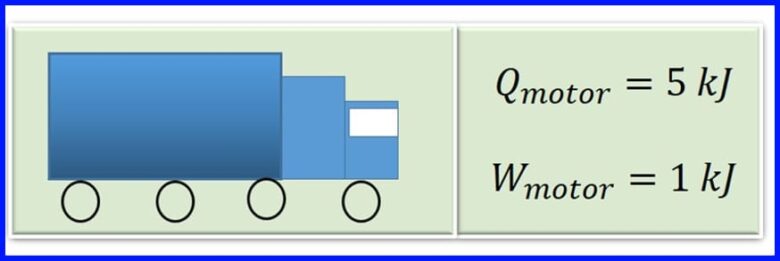
ਹੱਲ:

ਜਾਰੀ ਕੀਤੀ ਗਰਮੀ ਨੂੰ ਨਿਰਧਾਰਤ ਕਰਨ ਲਈ, ਇਹ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ ਕਿ ਥਰਮਲ ਮਸ਼ੀਨਾਂ ਵਿੱਚ ਸ਼ੁੱਧ ਕੰਮ ਸਿਸਟਮ ਵਿੱਚ ਸ਼ੁੱਧ ਗਰਮੀ ਦੇ ਬਰਾਬਰ ਹੁੰਦਾ ਹੈ. ਚਿੱਤਰ 14 ਵੇਖੋ.

ਐਂਟਰੋਪੀ:
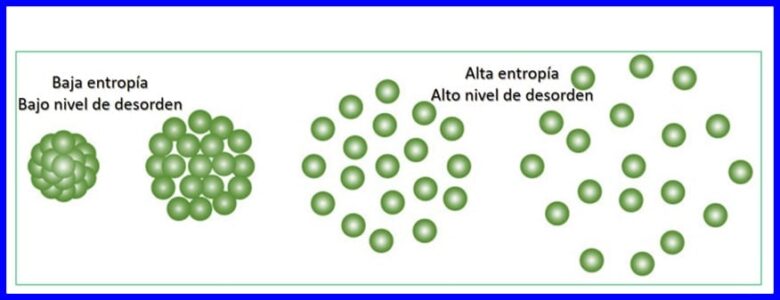
ਐਟਰੋਪੀ ਇੱਕ ਸਿਸਟਮ ਵਿੱਚ ਬੇਤਰਤੀਬੀ ਜਾਂ ਵਿਗਾੜ ਦੀ ਡਿਗਰੀ ਹੈ. ਐਂਟਰੋਪੀ itਰਜਾ ਦੇ ਉਸ ਹਿੱਸੇ ਦੀ ਮਾਤਰਾ ਨੂੰ ਸੰਭਵ ਬਣਾ ਦਿੰਦੀ ਹੈ ਜੋ ਕੰਮ ਪੈਦਾ ਕਰਨ ਲਈ ਨਹੀਂ ਵਰਤੀ ਜਾ ਸਕਦੀ, ਯਾਨੀ, ਇਹ ਥਰਮੋਡਾਇਨਾਮਿਕ ਪ੍ਰਕਿਰਿਆ ਦੀ ਅਟੱਲਤਾ ਨੂੰ ਮਾਪਣਾ ਸੰਭਵ ਬਣਾਉਂਦਾ ਹੈ.
ਹਰੇਕ energyਰਜਾ ਟ੍ਰਾਂਸਫਰ ਜੋ ਹੁੰਦਾ ਹੈ ਬ੍ਰਹਿਮੰਡ ਦੀ ਐਂਟਰੋਪੀ ਨੂੰ ਵਧਾਉਂਦਾ ਹੈ ਅਤੇ ਕੰਮ ਕਰਨ ਲਈ ਉਪਲਬਧ energyਰਜਾ ਦੀ ਮਾਤਰਾ ਨੂੰ ਘਟਾਉਂਦਾ ਹੈ. ਕੋਈ ਵੀ ਥਰਮੋਡਾਇਨਾਮਿਕ ਪ੍ਰਕਿਰਿਆ ਇਕ ਦਿਸ਼ਾ ਵਿਚ ਅੱਗੇ ਵਧੇਗੀ ਜੋ ਬ੍ਰਹਿਮੰਡ ਦੀ ਕੁੱਲ ਐਂਟਰੌਪੀ ਨੂੰ ਵਧਾਉਂਦੀ ਹੈ. ਚਿੱਤਰ 15 ਵੇਖੋ.
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਤੀਜਾ ਕਾਨੂੰਨ
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਜਾਂ ਨਰਸਟ ਪੋਸਟੁਲੇਟ ਦਾ ਤੀਜਾ ਕਾਨੂੰਨ
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਤੀਜਾ ਕਾਨੂੰਨ ਤਾਪਮਾਨ ਅਤੇ ਕੂਲਿੰਗ ਨਾਲ ਸਬੰਧਤ ਹੈ. ਇਹ ਦੱਸਦਾ ਹੈ ਕਿ ਪੂਰਨ ਸਿਫ਼ਰ ਤੇ ਇੱਕ ਪ੍ਰਣਾਲੀ ਦੀ ਐਂਟਰੋਪੀ ਇੱਕ ਨਿਸ਼ਚਿਤ ਨਿਰੰਤਰਤਾ ਹੈ. ਚਿੱਤਰ 16 ਵੇਖੋ.
ਸੰਪੂਰਨ ਜ਼ੀਰੋ ਸਭ ਤੋਂ ਹੇਠਲਾ ਤਾਪਮਾਨ ਹੈ ਜਿਸ ਤੋਂ ਬਾਅਦ ਹੁਣ ਕੋਈ ਘੱਟ ਉਪਾਅ ਨਹੀਂ ਹੁੰਦਾ, ਇਹ ਸਭ ਤੋਂ ਠੰਡਾ ਹੁੰਦਾ ਹੈ ਜੋ ਸਰੀਰ ਹੋ ਸਕਦਾ ਹੈ. ਸੰਪੂਰਨ ਜ਼ੀਰੋ 0 K ਹੈ, -273,15 ºC ਦੇ ਬਰਾਬਰ ਹੈ.

ਸਿੱਟਾ
ਚਾਰ ਥਰਮੋਡਾਇਨਾਮਿਕ ਸਿਧਾਂਤ ਹਨ. ਜ਼ੀਰੋ ਸਿਧਾਂਤ ਵਿਚ ਇਹ ਸਥਾਪਿਤ ਕੀਤਾ ਜਾਂਦਾ ਹੈ ਕਿ ਥਰਮਲ ਸੰਤੁਲਨ ਉਦੋਂ ਹੁੰਦਾ ਹੈ ਜਦੋਂ ਦੋ ਜਾਂ ਵਧੇਰੇ ਸਰੀਰ ਇਕੋ ਤਾਪਮਾਨ ਤੇ ਹੁੰਦੇ ਹਨ.
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਪਹਿਲਾ ਕਾਨੂੰਨ ਪ੍ਰਕ੍ਰਿਆਵਾਂ ਦਰਮਿਆਨ energyਰਜਾ ਦੀ ਸੰਭਾਲ ਨਾਲ ਸੰਬੰਧ ਰੱਖਦਾ ਹੈ, ਜਦੋਂ ਕਿ ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਦੂਜਾ ਕਾਨੂੰਨ ਘੱਟ ਤੋਂ ਲੈ ਕੇ ਸਭ ਤੋਂ ਵੱਧ ਐਂਟਰੋਪੀ ਦੀ ਦਿਸ਼ਾ-ਨਿਰਦੇਸ਼ਤਾ ਅਤੇ ਗਰਮੀ ਇੰਜਣਾਂ ਦੀ ਕੁਸ਼ਲਤਾ ਜਾਂ ਪ੍ਰਦਰਸ਼ਨ ਨਾਲ ਕੰਮ ਕਰਦਾ ਹੈ ਜੋ ਗਰਮੀ ਨੂੰ ਕੰਮ ਵਿੱਚ ਬਦਲਦੇ ਹਨ.
ਥਰਮੋਡਾਇਨਾਮਿਕਸ ਦਾ ਤੀਜਾ ਨਿਯਮ ਤਾਪਮਾਨ ਅਤੇ ਠੰ .ਾ ਕਰਨ ਨਾਲ ਸਬੰਧਤ ਹੈ, ਇਹ ਦੱਸਦਾ ਹੈ ਕਿ ਇਕ ਪ੍ਰਣਾਲੀ ਦਾ ਪੂਰਨ ਸਿਫ਼ਰ ਤੇ ਦਾਖਲਾ ਹੋਣਾ ਇਕ ਨਿਰੰਤਰ ਸਥਿਰ ਹੁੰਦਾ ਹੈ.