Principes thermodynamiques
Pour comprendre, de manière simple, le monde vaste et complexe de la thermodynamique, il est recommandé d'aller étape par étape en commençant par un examen des termes de base, une introduction aux principes de la thermodynamique, puis en étudiant plus en profondeur les lois de la thermodynamique, comment elles sont exprimés mathématiquement et ses applications.
Avec les quatre lois de la thermodynamique (loi zéro, première loi, deuxième loi et troisième loi), il est décrit comment fonctionnent les transferts et transformations d'énergie entre différents systèmes; étant la base pour comprendre de nombreux phénomènes physico-chimiques de la nature.
Revue des concepts de base
Nous vous invitons à voir l'article LA THERMODYNAMIQUE, ce qu'elle est et ses applications

Vous pouvez compléter ces informations avec l'article La puissance de la loi de Watt (Applications - Exercices) Pour le moment NOUS SUIVONS ...
Formes d'énergie
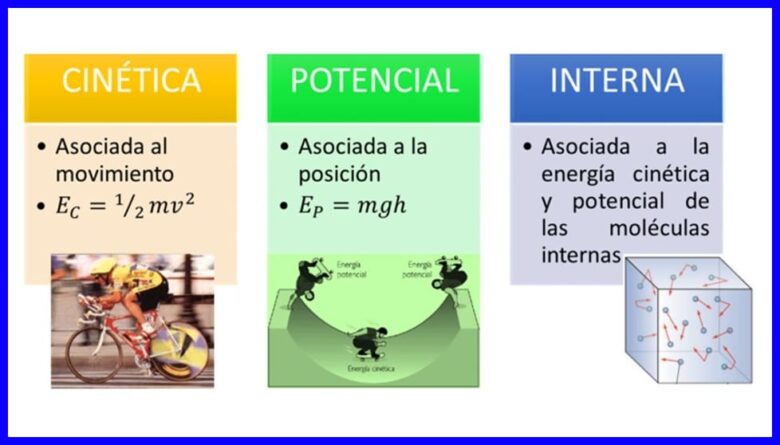
L'énergie, propriété des corps à se transformer en modifiant leur situation ou leur état, se présente sous de nombreuses formes, telles que énergie cinétique, énergie potentielle et énergie interne des corps. Voir la figure 1.
Travailler avec nous
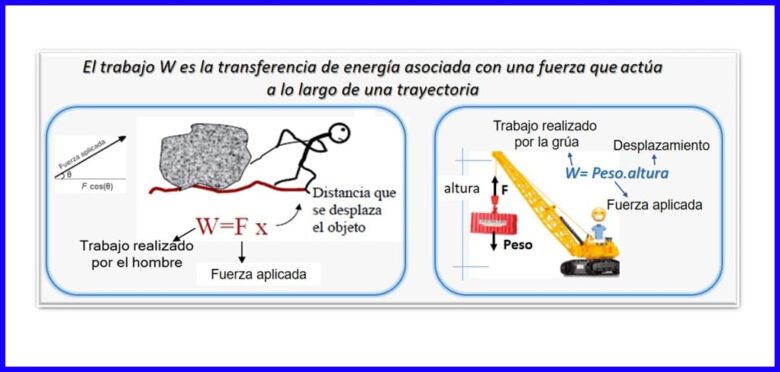
C'est le produit d'une force et d'un déplacement, tous deux mesurés dans la même direction. Pour calculer le travail, la composante de la force parallèle au déplacement de l'objet est utilisée. Le travail est mesuré en Nm, Joule (J), ft.lb-f ou BTU. Voir la figure 2.
Chaleur (Q)
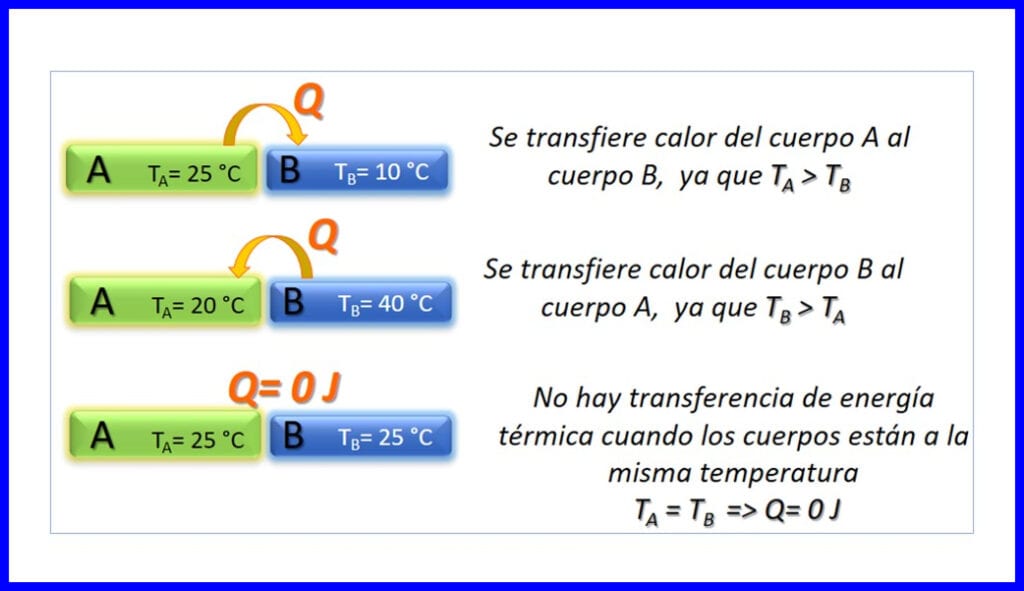
Transfert d'énergie thermique entre deux corps qui sont à des températures différentes, et cela ne se produit que dans le sens où la température diminue. La chaleur est mesurée en Joule, BTU, livre-pied ou en calories. Voir la figure 3.
Principes thermodynamiques
Loi zéro - Principe zéro
La loi zéro de la thermodynamique stipule que si deux objets, A et B, sont en équilibre thermique l'un avec l'autre et que l'objet A est en équilibre avec un troisième objet C, alors l'objet B est en équilibre thermique avec l'objet C.L'équilibre thermique se produit lorsque deux corps ou plus sont à la même température. Voir la figure 4.
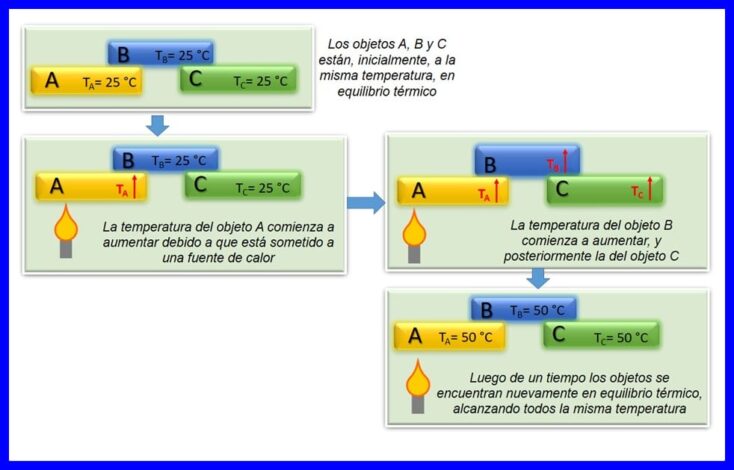
Cette loi est considérée comme une loi fondamentale de la thermodynamique. Il a été postulé comme "Loi zéro" en 1935, car il a été postulé après que les première et deuxième lois de la thermodynamique aient été faites.
1ère loi de la thermodynamique (principe de conservation de l'énergie)
Énoncé de la première loi de la thermodynamique:
La première loi de la thermodynamique, également connue sous le nom de principe de conservation de l'énergie, stipule que l'énergie n'est pas créée ou détruite, elle est seulement transformée en un autre type d'énergie, ou elle est transférée d'un objet à un autre. Ainsi, la quantité totale d'énergie dans l'univers ne change pas.
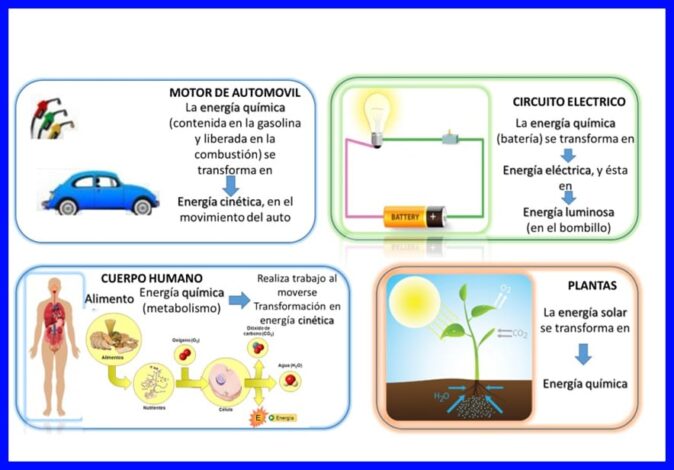
La première loi est remplie dans «tout», l'énergie est transférée et transformée en continu, par exemple, dans certains appareils électriques, tels que les mélangeurs et les mélangeurs, l'énergie électrique est transformée en énergie mécanique et thermique, dans le corps humain, ils sont transformés le produit chimique l'énergie de la nourriture qui est ingérée en énergie cinétique lorsque le corps est en mouvement, ou d'autres exemples tels que ceux illustrés à la figure 5.
Équation de la première loi de la thermodynamique:
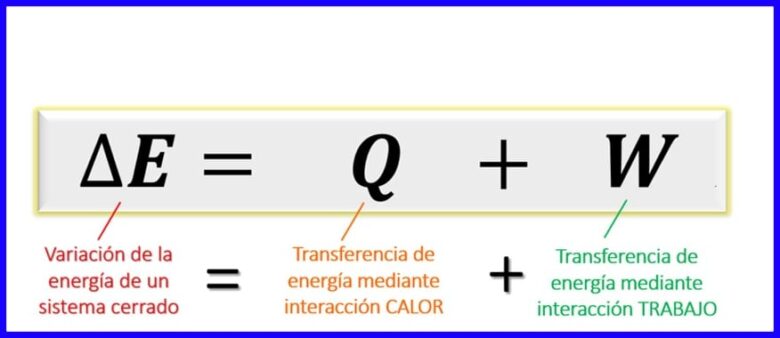
L'équation de la première loi au sein des principes thermodynamiques exprime l'équilibre qui doit exister entre les différents types d'énergie dans un processus donné. Puisque, dans les systèmes fermés [1], les échanges d'énergie ne peuvent être donnés que par le transfert de chaleur, ou par le travail effectué (par ou sur le système), il est établi que la variation d'énergie d'un système est égale à la somme des transferts d'énergie par la chaleur et par le travail. Voir la figure 6.
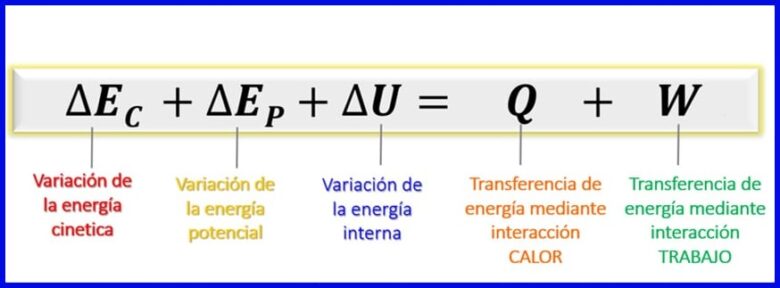
Considérant que les énergies considérées dans ce bilan énergétique sont l'énergie cinétique, l'énergie potentielle et l'énergie interne [1], le bilan énergétique des systèmes fermés reste tel qu'illustré à la figure 7.
- (Éc) Énergie cinétique , en raison du mouvement d'un corps;
- (ep) Énergie potentielle, en raison de la position d'un corps dans un champ gravitationnel;
- (OU) Énergie interne , en raison des contributions microscopiques de l'énergie cinétique et potentielle des molécules internes d'un corps.
Exercice 1.
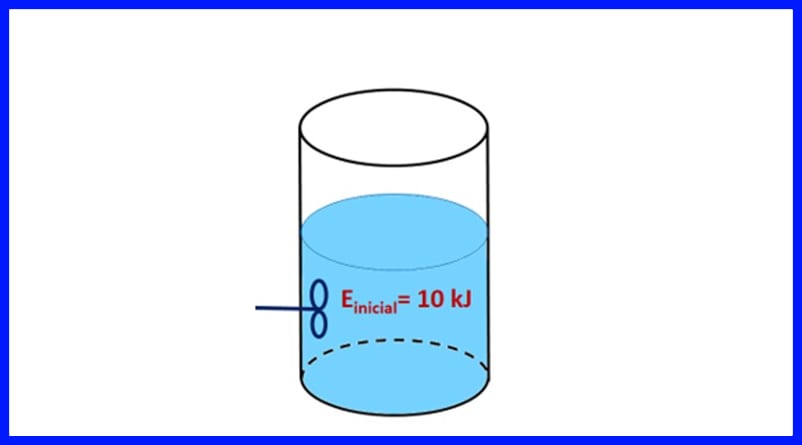
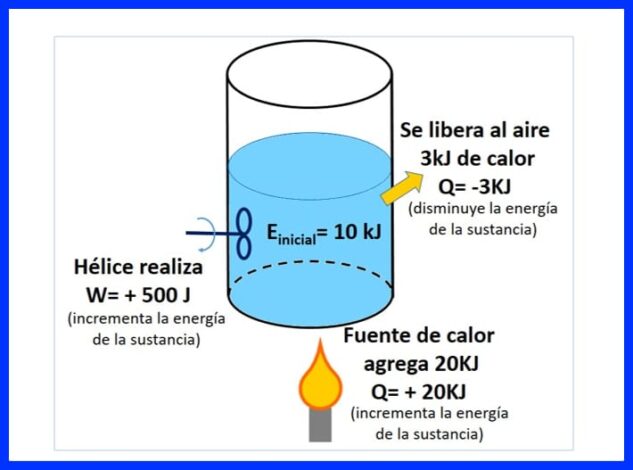
Un contenant scellé contient une substance d'une énergie initiale de 10 kJ. La substance est agitée avec une hélice qui effectue un travail de 500 J, tandis qu'une source de chaleur transfère 20 kJ de chaleur à la substance. De plus, 3 kJ de chaleur sont libérés dans l'air pendant le processus. Déterminez l'énergie finale de la substance. Voir la figure 8.
solution:
Dans la figure 9, vous pouvez voir la chaleur ajoutée par la source de chaleur, qui est considérée comme "positive" car elle augmente l'énergie de la substance, la chaleur qui est libérée dans l'air, négative car elle diminue l'énergie de la substance, et le le travail de l'hélice, qui a augmenté l'énergie, a pris un signe positif.
Sur la figure 10, le bilan énergétique est présenté, selon la première loi de la thermodynamique et l'énergie finale de la substance est obtenue.

Deuxième loi de la thermodynamique
Il existe plusieurs énoncés de la deuxième loi de la thermodynamique: Déclaration de Planck-Kelvin, Clausius, Carnot. Chacun d'eux montre un aspect différent de la seconde loi. En général, la deuxième loi de la thermodynamique postule:
- La direction des processus thermodynamiques, l'irréversibilité des phénomènes physiques.
- L'efficacité des machines thermiques.
- Entrez la propriété "entropie".
Direction des processus thermodynamiques:
Spontanément dans la nature, l'énergie circule ou est transférée de l'état d'énergie le plus élevé à l'état d'énergie le plus bas. La chaleur circule des corps chauds aux corps froids et non l'inverse. Voir la figure 11.

Efficacité ou performance thermique:
Selon la première loi de la thermodynamique, l'énergie n'est ni créée ni détruite, mais elle peut être transformée ou transférée. Mais dans tous les transferts ou transformations d'énergie, une partie de celle-ci n'est pas utile pour travailler. À mesure que l'énergie est transférée ou transformée, une partie de l'énergie initiale est libérée sous forme d'énergie thermique: l'énergie se dégrade, perd de sa qualité.
Dans toute transformation d'énergie, la quantité d'énergie obtenue est toujours inférieure à l'énergie fournie. L'efficacité thermique est la quantité de chaleur de la source qui est convertie en travail, le rapport entre l'énergie utile obtenue et l'énergie fournie lors d'une transformation. Voir la figure 12.

Machine thermique ou machine à chaleur:
La machine thermique est un appareil qui convertit partiellement la chaleur en travail ou en énergie mécanique, pour laquelle elle nécessite une source qui fournit de la chaleur à haute température.
Dans les machines thermiques, une substance telle que la vapeur d'eau, l'air ou le carburant est utilisée. La substance subit une série de transformations thermodynamiques de manière cyclique, de sorte que la machine peut fonctionner en continu.
Exercice 2.
Le moteur d'un véhicule cargo produit de la chaleur par combustion en brûlant de l'essence. Pour chaque cycle du moteur, la chaleur de 5 kJ est convertie en 1 kJ de travail mécanique. Quelle est l'efficacité du moteur? Quelle quantité de chaleur est libérée pour chaque cycle du moteur? Voir la figure 13
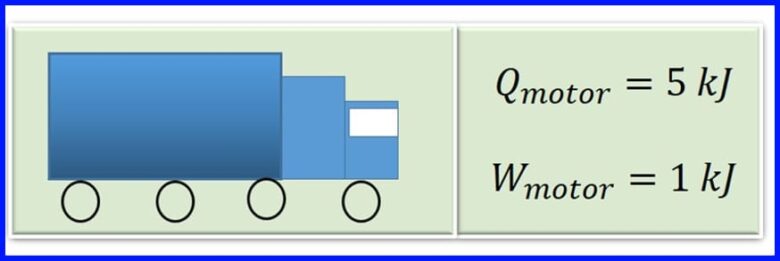
solution:

Pour déterminer la chaleur dégagée, on suppose que dans les machines thermiques, le travail net est égal au transfert de chaleur net vers le système. Voir la figure 14.

Entropía:
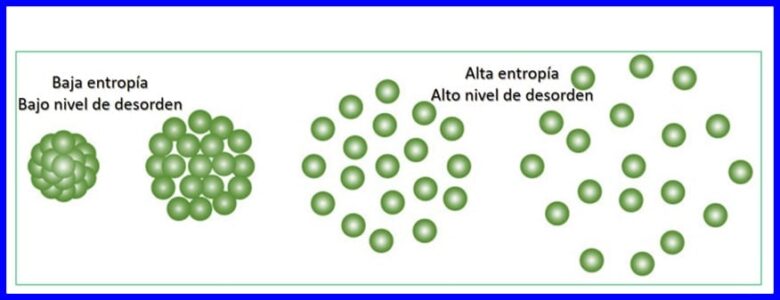
L'entropie est le degré de hasard ou de désordre dans un système. L'entropie permet de quantifier la part de l'énergie qui ne peut pas être utilisée pour produire du travail, c'est-à-dire qu'elle permet de quantifier l'irréversibilité d'un processus thermodynamique.
Chaque transfert d'énergie qui se produit augmente l'entropie de l'univers et réduit la quantité d'énergie utilisable disponible pour faire le travail. Tout processus thermodynamique se déroulera dans une direction qui augmente l'entropie totale de l'univers. Voir la figure 15.
3e loi de la thermodynamique
Troisième loi de la thermodynamique ou postulat de Nerst
La troisième loi de la thermodynamique est liée à la température et au refroidissement. Il déclare que l'entropie d'un système à zéro absolu est une constante définie. Voir la figure 16.
Le zéro absolu est la température la plus basse en dessous de laquelle il n'y a plus de mesure inférieure, c'est la plus froide qu'un corps puisse être. Le zéro absolu est 0 K, ce qui équivaut à -273,15 ºC.

Conclusion
Il existe quatre principes thermodynamiques. Dans le principe du zéro, il est établi que l'équilibre thermique se produit lorsque deux corps ou plus sont à la même température.
La première loi de la thermodynamique traite de la conservation de l'énergie entre les processus, tandis que la deuxième loi de la thermodynamique traite de la directivité de l'entropie la plus basse à la plus élevée, et de l'efficacité ou des performances des moteurs thermiques qui convertissent la chaleur en travail.
La troisième loi de la thermodynamique est liée à la température et au refroidissement, elle stipule que l'entropie d'un système à zéro absolu est une constante définie.